
石油化工的重要原料CxHy可以合成很多有机化合物,以下是CxHy合成物质E和J 的流程图:

已知:Ⅰ.下列反应中R、R′代表烃基

Ⅱ.J的分子式为C4H4O4 ,是一种环状化合物。
(1)在CxHy同系物中,所有碳原子一定共平面且碳原子数最多的分子的名称是
(2)写出G中的官能团 名称 ,H的分子式是 。
(3)下列说法正确的是
a.CxHy和苯都能使溴水褪色,原理相同
b.反应②和反应④的反应类型均为加成反应
c.C能与Na、NaOH、NaHCO3反应
d. E是一种水溶性很好的高分子化合物
e.J在酸性或碱性环境中均能水解
(4)K是J的同分异构体,且1 mol K与足量的NaHCO3溶液反应可放出2mol CO2气体,请写出一种符合条件K的结构简式
(5)写出反应⑤的化学方程式
(6)D有多种同分异构体,与D具有相同官能团的还有 种(不考虑顺反异构),其中核磁共振氢谱有3组吸收峰,且能发生银镜反应的结构简式是
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:2015-2016学年辽宁省协作校高二下期末化学试卷(解析版) 题型:选择题
已知:乙醇可被强氧化剂氧化为乙酸,BrCH2CH=CHCH2Br可经三步反应制取HOOCCHClCH2COOH,发生反应的类型依次是( )
A.水解反应、加成反应、氧化反应
B.加成反应、水解反应、氧化反应
C.水解反应、氧化反应、加成反应
D.加成反应、氧化反应、水解反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省泰安市高一下学期期末考试化学试卷(解析版) 题型:选择题
向甲、乙、丙、丁四个容积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小的顺序排列正确的是( )
甲.在500℃时,10 mol SO2和5 mol O2反应
乙.在500℃时,用V2O5做催化剂,10 mol SO2和5 mol O2反应
丙.在450℃时,8 mol SO2和5 mol O2反应
丁.在500℃时,8 mol SO2和5 mol O2反应
A.甲、乙、丙、丁
B.乙、甲、丙、丁
C.乙、甲、丁、丙
D.丁、丙、乙、甲
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省泰安市高一下学期期末考试化学试卷(解析版) 题型:选择题
有5种单核粒子,它们分别是4018□、4019□、4019□+、4020□2+、4120□(□内元素符号未写出),则它们所属元素的种类有( )
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二下期末化学试卷(解析版) 题型:选择题
由甲酸甲酯、葡萄糖、乙醛、丙酸四种物质组成的混合物,已知其中氧元素的质量分数为37%,则氢元素的质量分数为 ( )
A.9% B.12% C.15% D. 23%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二下期末化学试卷(解析版) 题型:选择题
线型弹性材料“丁苯吡橡胶”的结构简式如下:
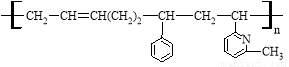
其单体可能是:
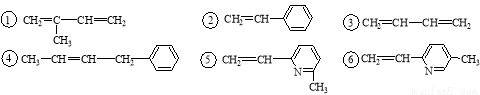
正确的组合是 ( )
A.①②⑥ B.②③⑤ C.②③⑥ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下期末化学试卷(解析版) 题型:实验题
回归、改进、拓展教材实验,是高考化学实验考查的常见形式。
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究。基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理。
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性。
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式__________________________________。
(2)①该催化剂中铁元素的化合价为 。
②下图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是 。

II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):
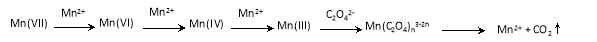
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+ 对该反应有催化作用
假设3:K+ 对该反应有催化作用
【设计、完成实验】
(3)称取 g草酸晶体(H2C2O4·2H2O),配制500 mL 0.10 mol/L H2C2O4溶液。在上述过程中必须用到的2种定量仪器是托盘天平和
(4)完成探究,记录数据
实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
仔细阅读分析表中数据,回答问题:
x = mL,假设__________成立(填“1” 、“2”或“3”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海省高一下期末化学试卷(解析版) 题型:选择题
下列关于碱金属的叙述正确的是 ( )
A. 随着核电荷数增加,它们的密度逐渐减小
B. 随着核电荷数增加,单质的熔点、沸点升高
C. 随着核电荷数的增加,单质与水反应的剧烈程度增大
D. 随着核电荷数增加,离子的氧化性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com