
 T℃时,在V L恒容密闭容器中加入足量的TaS2(s)和1mol I2(g),发生反应TaS2(s)+2I2(g)?TaI4(g)+S2(g)△H>0.t min时生成0.1mol TaI4.下列说法正确的是( )
T℃时,在V L恒容密闭容器中加入足量的TaS2(s)和1mol I2(g),发生反应TaS2(s)+2I2(g)?TaI4(g)+S2(g)△H>0.t min时生成0.1mol TaI4.下列说法正确的是( )A、0~t min内,v(I2)=
| ||
B、若T℃时反应的平衡常数K=1,则平衡时I2的转化率为
| ||
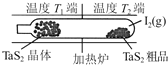
| C、图中制备TaS2晶体过程中循环使用的物质是S2(g) | ||
| D、图中T1端得到纯净TaS2晶体,则温度T1<T2 |
| △c |
| △t |
| △c |
| △t |
| ||
| tmin |
| 0.2 |
| Vt |
| (0.5x)2 |
| (1-x)2 |
| 2 |
| 3 |
| 2 |
| 3 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
温度为T时,向2.0L恒容密闭容器中充入2.0mol NO2,反应2NO2(g)?N2O4(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50s的平均速率为v(PCl3)=0.0032mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol?L-1,则反应的△H<0 |
| C、相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,达到平衡前v(正)>v(逆) |
| D、相同温度下,起始时向容器中充入2.0mol PCl3、2.0mol Cl2,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省南京市、淮安市高三第二次模拟考试化学试卷(解析版) 题型:选择题
T℃时,在V L恒容密闭容器中加入足量的TaS2(s)和1 mol I2(g),发生反应TaS2(s)+2I2(g)  TaI4(g)+S2(g) △H>0。t min时生成0.1 mol TaI4。下列说法正确的是
TaI4(g)+S2(g) △H>0。t min时生成0.1 mol TaI4。下列说法正确的是

A.0~t min内,v(I2)= mol·L-1·min-1
mol·L-1·min-1
B.若T℃时反应的平衡常数K=1,则平衡时I2的转化率为2/3
C.如图制备TaS2晶体过程中循环使用的物质是S2(g)
D.图中T1端得到纯净TaS2晶体,则温度T1<T2
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市朝阳区高三第二次综合练习理综化学试卷(解析版) 题型:选择题
温度为T时,向2 L恒容密闭容器中充入1 mol
PCl5,发生PCl5(g)  PCl3(g)
+ Cl2(g)反应。反应过程中c(Cl2) 随时间变化的曲线如下图所示,下列说法不正确的是
PCl3(g)
+ Cl2(g)反应。反应过程中c(Cl2) 随时间变化的曲线如下图所示,下列说法不正确的是

A.反应在0 ~50 s 的平均速率v(Cl2) =1.6×10-3mol/(L·s)
B.该温度下,反应的平衡常数K = 0.025
C.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol/L,则该反应的ΔH <0
D.反应达平衡后,再向容器中充入 1 mol PCl5,该温度下再达到平衡时,0.1 mol/L<c(Cl2)<0.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com