
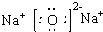 ,它在水溶液中,或熔融状态下能完全电离的化合物,是强电解质;
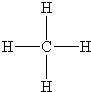
,它在水溶液中,或熔融状态下能完全电离的化合物,是强电解质; ,它难溶于水,只存在甲烷分子,不导电,属于非电解质,
,它难溶于水,只存在甲烷分子,不导电,属于非电解质,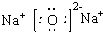 ;
;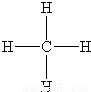 ;碱性;F-+H2O?HF+OH-.
;碱性;F-+H2O?HF+OH-.

科目:高中化学 来源: 题型:
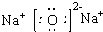

查看答案和解析>>
科目:高中化学 来源: 题型:
有下列八种物质:A.硫酸亚铁;B.稀硫酸;C.过氧化钠;D.水玻璃;E、烧碱溶液;F、浓氨水;G、氯化铵;H、硝酸钾。按要求回答问题:
⑴其中属于电解质的有________________________________(用各物质的序号);
⑵物质的量浓度均为0.1mol·L-1的 D.F、G、H四种物质的溶液,按溶液pH由小到大排列的顺序为(将各物质的序号用“<”连接表示)_________________;
⑶在足量C中通入CO2气体,写出反应的化学方程式并标明电子得失情况;
____________________________________________________________________;
⑷将E逐滴滴入A的溶液中,请用简单的文字和离子方程式说明所发生的现象及该过程的化学原理______________________________________________________
________________________________________________________________________________________________________________________________________________;
⑸将物质的量浓度均为0.02mol·L-1的 B.E等体积混合,所得溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年广东省高州市高三上学期期末考试(理综)化学部分 题型:填空题
有下列八种物质:A.硫酸亚铁;B.稀硫酸;C.过氧化钠;D.水玻璃;E、烧碱溶液;F、浓氨水;G、氯化铵;H、硝酸钾。按要求回答问题:
⑴其中属于电解质的有________________________________(用各物质的序号);
⑵物质的量浓度均为0.1mol·L-1的 D.F、G、H四种物质的溶液,按溶液pH由小到大排列的顺序为(将各物质的序号用“<”连接表示)_________________;
⑶在足量C中通入CO2气体,写出反应的化学方程式并标明电子得失情况;
____________________________________________________________________;
⑷将E逐滴滴入A的溶液中,请用简单的文字和离子方程式说明所发生的现象及该过程的化学原理______________________________________________________
________________________________________________________________________________________________________________________________________________;
⑸将物质的量浓度均为0.02mol·L-1的 B.E等体积混合,所得溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com