
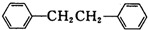 ����һ����Ҫ���л��ϳ��м��壬ʵ���ҿ��ñ���1��2һ�������飨ClCH2CH2Cl��Ϊԭ�ϣ�����ˮAlCl3���¼����Ƶã�����ȡ����Ϊ��
����һ����Ҫ���л��ϳ��м��壬ʵ���ҿ��ñ���1��2һ�������飨ClCH2CH2Cl��Ϊԭ�ϣ�����ˮAlCl3���¼����Ƶã�����ȡ����Ϊ��
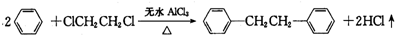
| ���� | ��Է������� | �ܶ�/��g•cm-3�� | �۵�/�� | �е�/�� | �ܽ��� |
| �� | 78 | 0.88 | 5.5 | 80.1 | ����ˮ�������Ҵ� |
| 1��2-���Ȼ��� | 99 | 1.27 | -35.3 | 83.5 | ����ˮ�����ܱ� |
| ��ˮ�Ȼ��� | 133.5 | 2.44 | 190 | 178�������� | ��ˮ�ֽ⣬�ܱ� |
| ���� | 182 | 0.98 | 52 | 284 | ����ˮ�����ܱ� |
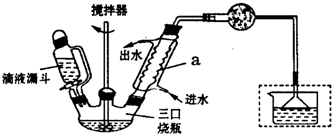
���� ��1������ʵ��װ��ͼ��֪����ʵ������Ũ������������̷�Ӧ�������������������Ȼ��⡢ˮ�����ʣ����ñ���ʳ��ˮ���Ȼ��⣬����Ũ����������������Ӧ�Ƶ��Ȼ�������Ӧ��β�������������գ�Ϊ��ֹ�Ȼ���������������Һ�е�ˮ������Ӧ��������E���β������װ�ã�
��2������HCl��Al��Ӧ����H2��H2��Cl2��ϼ���ʱ�ᷢ����ը��������
��3��AlCl3�����ɹ��������Թܶ������ݴ˻ش�
��4������ʵ���������ص���ȷ�������ƣ����Һ��©������ͨ��Һ©�����ص��Լ�ʹ��ԭ�����ش�
��5��ϴ�Ӳ����У��ڶ���ˮϴ��Ҫ�dz�ȥ�Ȼ����������̼���ƣ���ϴ�������������ϴ�Ӻ����������ˮ����þ���壬Ŀ�������ղ�Ʒ��������ˮ�֣�Ҳ�������Ȼ��ƴ��棻
��6����ѹ���ɽ��ͷе㣬����ʵ��Ŀ���Լ����ʵ��۷е����ش�
��7��120mL�����ܶ�0.88g/mL�������ʵ���Ϊ$\frac{120��0.88}{78}$mol=1.35mol��10.2mL1��2-������������ʵ���Ϊ$\frac{10.7��1.27}{99}$mol=0.137mol�����ݱ���1��2-��������Ϊԭ���Ʊ������ķ���ʽ��֪�������������Բ�Ʒ�����۲���Ϊ0.137mol��182g/mol=24.98g�����ݲ���=$\frac{ʵ�ʲ���}{���۲���}$��100%���㣮
��� �⣺��1��ʵ�����Ʊ���ˮ�Ȼ�������Ҫ����ȡ��������2װ�ã���������3���ڳ�ȥ�����е��Ȼ��⣬4���ڸ���������������ˮ�Ȼ�������ʪ����������ˮ����FeCl3•nH2O������5��ֹ�����е�ˮ�������룬ͬʱ����δ��Ӧ����������ֹ��Ⱦ������������������˳��Ϊd��e��f��g��h��a��b��c��
�ʴ�Ϊ��f��g��h��a��b��c��
��2��������װ����Dȥ��������װ�ú��Լ����䣬�����Ʊ���ˮAlCl3����Ϊ�Ƶõ�Cl2�л��е�HCl��Al��Ӧ����H2��H2��Cl2��ϼ���ʱ�ᷢ����ը��
�ʴ�Ϊ�������У��Ƶõ�Cl2�л��е�HCl��Al��Ӧ����H2��H2��Cl2��ϼ���ʱ�ᷢ����ը��
��3��Ϊ�˷�ֹAlCl3�����ɹ��������Թܶ�������Ӳ�ʲ���������ƿ֮���ôֵ������ӣ�
�ʴ�Ϊ����Ӳ�ʲ���������ƿ֮���ôֵ������ӣ���ֹAlCl3�����ɹ�����ɶ�����
��4������ʵ���������ص㣬֪����װ�õ������ǣ����������ܣ�����ͨ��Һ©����ȣ�ʹ�õ�Һ©�����ŵ��ǿ���ʹҺ��˳�����£�
�ʴ�Ϊ�����������ܣ�����ʹҺ��˳�����£�
��5��ϴ�Ӳ����У��ڶ���ˮϴ��Ҫ�dz�ȥ�Ȼ����������̼���ƣ���ϴ�������������ϴ�Ӻ����������ˮ����þ���壬Ŀ�������ղ�Ʒ��������ˮ�֣�Ҳ�������Ȼ��ƴ��棬����ˮ�������������
�ʴ�Ϊ��ϴ��Na2CO3����ϴ���������������ˮ�������������
��6����ѹ����ʱ����ѹ���ɽ��ͷе㣬�����¶ȹ��ߣ����¸���Ӧ�ķ������������ʵ��۷е�ĸߵͣ���Ҫ��Ϳ����¶���83.5�棬
�ʴ�Ϊ��83.5�棻
��7��120mL�����ܶ�0.88g/mL�������ʵ���Ϊ$\frac{120��0.88}{78}$mol=1.35mol��10.2mL1��2-������������ʵ���Ϊ$\frac{10.7��1.27}{99}$mol=0.137mol�����ݱ���1��2-��������Ϊԭ���Ʊ������ķ���ʽ��֪�������������Բ�Ʒ�����۲���Ϊ0.137mol��182g/mol=24.98g������=$\frac{ʵ�ʲ���}{���۲���}$��100%=$\frac{28.2g}{24.98g}$��100%=72.85%��
�ʴ�Ϊ��72.85%��
���� ���⿼���Ʊ�ʵ�鷽����ƣ�Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ�������ѧ���ķ�����ʵ�������Ŀ��飬��ȷԭ���ǽ���ؼ���ע�������ػ���ʵ�鷽���Ͳ����İ��գ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��2HI��g��?H2��g��+I2��g��ƽ����ϵ����ѹǿʹ��ɫ���� | |
| B�� | ��ӦCO��g��+NO2��g��?CO2��g��+NO��g����H��0�����¶�ʹƽ�����淽���ƶ� | |
| C�� | �ϳɰ���Ӧ��N2��g��+3H2��g��?2NH3��g����H��0��Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ | |
| D�� | ����ˮ�д�������ƽ�⣺Br2��g��+H2O��l��?HBr��aq��+HBrO��aq����������NaOH��Һ����ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 64.0 | 50.7 | 42.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȣ��棩 | |
| 500 | 800 | ||
| ��2H2��g��+CO��g��?CH3OH��g�� | K1 | 2.5 | 0.15 |
| ��H2��g��+CO2��g��?H2O ��g��+CO��g�� | K2 | 1.0 | 2.50 |
| ��3H2��g��+CO2��g��?CH3OH��g��+H2O ��g�� | K3 | ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
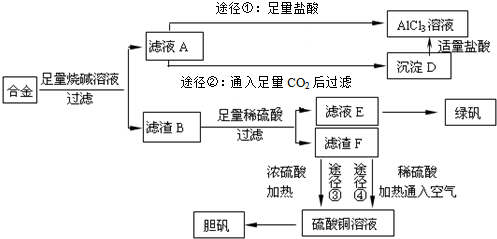
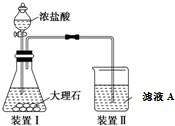
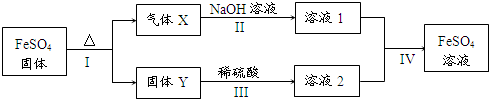
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
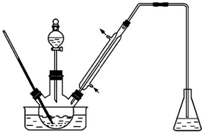 ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ��ʵ��װ����ͼ��������ʵķе����������
ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ��ʵ��װ����ͼ��������ʵķе����������| ���� | �е�/�� | ���� | �е�/�� |
| �� | 58.8 | 1��2-�������� | 83.5 |
| ����ȩ | 179 | ���屽��ȩ | 229 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
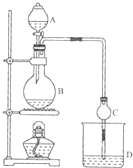 ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A�з���Ũ���ᣬB�з����Ҵ�����ˮ�����ƣ�D�з��б���̼������Һ�� ��֪
ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A�з���Ũ���ᣬB�з����Ҵ�����ˮ�����ƣ�D�з��б���̼������Һ�� ��֪| �Լ� | ���� | �Ҵ� | ���� | �������� |
| �е�/�� | 34.7 | 78.5 | 118 | 77.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com