解:(1)分离溶液中的Cl-,应加入AgNO3,分离溶液中的SO42-,应加入BaCl2[或Ba(NO3)2],如先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3,所以试剂1为BaCl2[或Ba(NO3)2],试剂2为AgNO3,试剂3为Na2CO3,试剂4为HNO3,故答案为:氯化钡溶液或硝酸钡溶液;硝酸银溶液;稀硝酸;
(2)加入过量的BaCl2[或Ba(NO3)2],在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,反应后溶液中存在过量的Ag+、Ba2+,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,
故答案为:除去溶液中过量的Ba2+、Ag+;
(3)分离固体和液体用过滤,操作①的名称是过滤,从溶液中获得固体,应将溶液进行蒸发,然后冷却结晶、最后过滤可得固体,故答案为:蒸发、冷却结晶、过滤.
分析:如先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3.
点评:本题考查物质的分离提纯操作,题目难度中等,本题注意Cl-、SO42-的性质,把握除杂原则,提纯时不能引入新的杂质,注意把握实验的先后顺序.

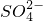 和
和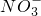 的相互分离,实验过程如下:
的相互分离,实验过程如下:


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案