
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:单选题
下列各组离子,在指定条件下,一定能大量共存的是
①某无色透明的酸性溶液中:Cl-、Na+、CrO42-、SO42-;
②水电离产生的c(H+)=10-12mol/L的溶液中:K+、Ba2+、Cl-、NO3-;
③使紫色石蕊试液变红的溶液中:Fe2+、Mg2+、NO3-、Cl-;
④加入过量NaOH溶液后可得到澄清溶液:K+、Ba2+、HCO3-、Cl-;
⑤c(H+)<c(OH-)的溶液中:ClO-、Cl-、K+、Na+;
⑥在酸性高锰酸钾溶液中:Na+、NH4+、I-、ClO-;
⑦能使pH试纸变深蓝色的溶液中:Na+、AlO2-、K+、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
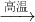 2Fe2O3+8SO2,若a g FeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
2Fe2O3+8SO2,若a g FeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室需要500ml 0.4mol?L-1的NaOH溶液,配制时:
实验室需要500ml 0.4mol?L-1的NaOH溶液,配制时:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com