
【题目】下列有关金属元素特征的叙述正确的是( )
A.金属元素的原子只有还原性,离子只有氧化性
B.金属元素的单质在常温下均为金属晶体
C.金属元素在不同的化合物中的化合价均不同
D.金属元素在一般化合物中只显正价
科目:高中化学 来源: 题型:
【题目】为了验证木炭可被浓H2SO4氧化成CO2 , 选用下图所示仪器(内含物质)组装成实验装置: 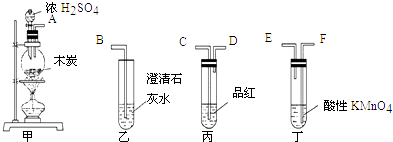
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):接 , 接 , 接;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中 , 丙中;
(3)丁中酸性KMnO4溶液的作用是;
(4)写出甲中反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘微溶于水,易溶于四氯化碳和酒精且碘易升华。现要将碘水中的碘分离出来,下列说法合理的是
A.碘易升华,可采用加热的方法将碘从溶液中升华出来
B.碘易溶于四氯化碳和酒精,所以可选用两种试剂中的任意一种进行萃取
C.四氯化碳比水重,酒精比水轻,所以用四氯化碳进行萃取比用酒精好
D.四氯化碳不溶于水,酒精溶于水,所以用四氯化碳萃取,不能用酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果.如利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
I、CH4(g)═C(s)+2H2(g)△H=+75.0kJmol﹣1
II、CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.0kJmol﹣1
III、CO(g)+H2(g)═C(s)+H2O(g)△H=﹣131.0kJmol﹣1
(1)反应CO2(g)+CH4(g)═2CO(g)+2H2(g)的△H=kJmol﹣1 .
(2)固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲. 
①同温度下CO2的平衡转化率(填“大于”或“小于”)CH4的平衡转化率,其原因是
②高温下进行该反应时常会因反应I生成“积碳”(碳单质),造成催化剂中毒,高温下反应I能自发进行的原因是 .
(3)一定条件下Pd﹣Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图乙所示,该反应的化学方程式为
(4)CO常用于工业冶炼金属,如图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图.下列说法正确的是
A.工业上可以通过增高反应装置来延长矿石和
CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于
提高CO的利用率
D.CO还原PbO2的反应△H>0
(5)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2 ![]() 2CO+O2 , 则其阳极的电极反应式为 .
2CO+O2 , 则其阳极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:


(1)等质量的上述物质完全燃烧,消耗氧气最多的是__________(填字母),等物质的量的上述物质完全燃烧,生成CO2最多的是__________(填字母)。
(2)能使酸性KMnO4溶液褪色的是_______________(填字母)。
(3)G与氢气完全加成后,所得产物的一卤代物有_______种。
(4)写出实验室制取D的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2 mol有机物和0.55 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8 g;再通过灼热CuO充分反应后,固体质量减轻4.8 g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加26.4 g。
(1)燃烧后产生CO的物质的量___________mol。
(2)该有机物的分子式_____________。
(3)若该有机物能与碳酸钠反应,试写出该有机物的结构简式___________。
(4)若该有机物呈中性且能水解,也能发生银镜反应。名称为____________。
(5)能发生银镜反应,又能与金属钠产生氢气,则同分异构体共有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10; X和Ne原子的核外电子数相差1; Y的单质是一种常见的半导体材料; Z的非金属性在同周期元素中最强。下列说法正确的是

A. 对应简单离子半径: X>W
B. 对应气态氢化物的稳定性Y
C. 化合物XZW既含离子键,又含共价键
D. Y的氧化物与乙的氢化物、X的最高价氧化物对应的水化物的溶液均能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)H2(g)+I2(g),2s时生成0.1mol H2 , 则以HI表示该时段的化学反应速率是( )
A.0.05 molLˉ1sˉ1
B.0.1 molLˉ1sˉ1
C.0.2 molLˉ1sˉ1
D.0.8 molLˉ1sˉ1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com