
将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反 应的HCl为0.08 mol,放出标准状况下的气体0.224 L。则下列判断中正确的是
应的HCl为0.08 mol,放出标准状况下的气体0.224 L。则下列判断中正确的是
A.原混合物中n(Fe)∶n(Fe2O3)=2∶1
B.向溶 液中滴入KSCN溶液,显血红色
液中滴入KSCN溶液,显血红色
C.无法计算原混合物的质量
D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是
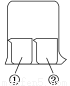
①中的物质 | ②中的物质 | 预测①的现象 | |
A | 淀粉?KI溶液 | 浓硝酸 | 无明显变化 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第二次月考化学试卷(解析版) 题型:填空题
(每空2分,共10分)
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、KCl等混合而成,为检验它们,做了如下实验:
①将固体混合物溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解。
试判断:
(1)固体混合物中肯定有 ,肯定没有 ,可能有 。
(2)写出有关的离子方程式:实验② ;实验③ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
常温下,pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶 液的体积之比为
A.11:1 B.9:1 C.1:11 D.1:9
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三10月月考化学试卷(解析版) 题型:选择题
有一块铝铁合金,将其溶解于足量盐酸中,再加入足量NaOH溶液,在空气中静置至红褐色沉淀不再增加时,将沉淀滤出再灼烧至恒重,得到残留物的质量与原合金质量相同,则合金中铝的质量分数是
A、22.2% B、30% C、75.5% D、80.6%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第一次月考化学试卷(解析版) 题型:选择题
在某K2SO4和Fe2(SO4)3的混合溶液中, Fe3+物质的量浓度为0.1 mol/L,SO42-物质的量浓度为0.3 mol/L,则K+的物质的量浓度为
A.0.6mol/L B.0.3mol/L C.0.2mol/L D.0.15mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
25℃时,Kw=1.0×10﹣14;100℃时,Kw=5.5×10﹣13.下列说法正确的是
A.100℃时,pH=12的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7
B.25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7
C.25℃时,0.2 mol/L NaOH溶液与0.2 mol/L CH3COOH恰好中和,所得溶液的pH=7
D.25℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期10月月考化学试卷(解析版) 题型:实验题
(14分)茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以测定某品牌茶叶中钙元素的质量分数并检验铁元素的存在(已知CaC2O4为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作:
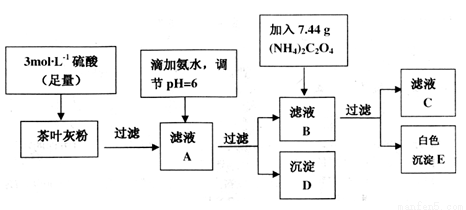
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
离子 |
|
|
完全沉淀时的pH | 13 | 3.7 |
实验前要先将茶叶样品高温灼烧成灰粉,需用到的仪器有__________________。
①酒精灯 ②蒸发皿 ③坩埚 ④泥三角 ⑤三脚架 ⑥铁架台
(2)写出从滤液A→沉淀D的离子反应方程式的是________________________。
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试判断沉淀D已经洗涤干净的方法是___________________________。
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:
5C2O42-+2MnO4-+16+=10CO2↑+2Mn2++8H2O。现将滤液C稀释至500 mL,再取其中的25.00 mL溶液,用硫酸酸化后,用0.1000mol·L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00 mL。
①此步操作过程中一定需要用到下列哪些仪器(填写序号)_____________;

②达到滴定终点时,溶液的颜色变化是_______________;
③滴定到终点,静置后如图读取KMnO4标准溶液刻度数据,则测定钙元素含量将__________(填“偏高”、“偏低”、“无影响”)。
(5)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及实验现象是______________。
(6)原茶叶中钙元素的质量分数为____________________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省牡丹江市高三9月月考化学试卷(解析版) 题型:选择题
下列除杂方法正确的是
A.SiO2中含Al2O3杂质,可以加入足量NaOH溶液然后过滤除去
B.NH4Cl固体中混有少量的单质I2,可用加热方法将I2除去
C.CO2中含有SO2杂质,可以通过盛有饱和Na2CO3溶液的洗气瓶除去
D.NaHCO3溶液中含有Na2SiO3杂质,可以通入足量的CO2,然后过滤除去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com