
����Ŀ����֪2SO2��g��+O2��g��2SO3��g����H=��198.0 kJmol��1 �� ����500��ʹ����������£���Ӧ���ݻ��̶����ܱ������н��У������й�˵����ȷ���ǣ� ��
A.�÷�Ӧ�����£���ʼʱ�������г���2molSO2��1molO2 �� ��Ӧƽ��ʱ�������ͷ�198.0 kJ������
B.�ﵽƽ��ʱ��SO2��SO3��Ũ��һ�����
C.��Ӧ��ϵ�У����������ܶȱ��ֲ��䣬��Ӧ�ﵽƽ��
D.����ѹǿ�������¶������ڼӿ췴Ӧ���ʣ��������¶ȶ�ƽ��ת���ʲ���
���𰸡�D
���������⣺A�����淴Ӧ������ȫת�����������������£�2molSO2��1molO2��Ϸ�Ӧ���ų�������С��198.0kJ����A����
B��ת���ʺ���ʼŨ��δ֪����Ӧ��ƽ��ʱ��SO2��SO3��Ũ�ȹ�ϵ��ȷ������ȷ������Ũ�ȱ��ֲ��䣬��B����
C��������������䣬��Ӧ��ϵ�ж������壬�������������䣬���� ![]() ��֪��Ӧ������������ܶ�ʼ�ղ��䣬������Ϊ��ƽ��ı�־����C����
��֪��Ӧ������������ܶ�ʼ�ղ��䣬������Ϊ��ƽ��ı�־����C����
D������ѹǿ�������¶ȷ�Ӧ���ʶ��ӿ죬����ѹǿƽ�������������С�ķ����ƶ��������������ת���ʣ����������ȷ����ƶ����淽���ƶ���������ת���ʣ���D��ȷ��
��ѡD��
�����㾫�����������⣬������Ҫ�˽⻯ѧƽ��״̬���ʼ�����(��ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч��)��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�m g����A��n g����B��������ȣ�����˵������ȷ���ǣ�������
A.��״���£�ͬ���������A������B��������m��n
B.25�棬101KPaʱ��1Kg����A��1Kg����B�ķ�������Ϊn��m
C.ͬ��ͬѹ�£�����A������B�ܶȱ�Ϊn��m
D.��״���£���������A��B�������Ϊn��m
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������AlON����ԭ�Ӿ��壬��һ�ֳ�ǿ�����ϣ������ɷ�ӦAl2O3+C+N2 ![]() 2AlON+CO�ϳɣ������й�˵����ȷ���ǣ� ��
2AlON+CO�ϳɣ������й�˵����ȷ���ǣ� ��
A.���������е��Ļ��ϼ��ǩ�3
B.��Ӧ����������ͻ�ԭ��������ʵ���֮����1��2
C.��Ӧ��ÿ����5.7gAlONͬʱ����1.12LCO
D.AlON��CO�Ļ�ѧ�����Ͳ�ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A.ͭ����������Һ��Ӧ��Cu+Ag+=Cu2++Ag
B.̼��������ᷴӦ�� ![]() +2H+=CO2��+H2O
+2H+=CO2��+H2O
C.����������������Һ��Ӧ��H++ ![]() +Ba2++OH=BaSO4��+H2O
+Ba2++OH=BaSO4��+H2O
D.Ba(OH)2��CuSO4��Һ��Ӧ��Cu2++ ![]() +Ba2++2OH=BaSO4��+Cu(OH)2��
+Ba2++2OH=BaSO4��+Cu(OH)2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƿ����Ҫ�������¶���Ũ����������ѹǿ���̶�������ʽ����ʽ �����еģ� ��
A. �٢ۢ� B. �ڢܢ� C.�ۢݢ� D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2A��g��+B��g��=3C��g��+4D��g���У���ʾ�÷�Ӧ���������ǣ� ��
A.v��A��=0.5molL��1 �� mim��1
B.v��B��=0.3molL��1 �� mim��1
C.v��C��=0.8molL��1 �� mim��1
D.v��D��=1.0molL��1 �� mim��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ���Cl����SO42����CO32����NH4+��Fe3+��Fe2+��Na+ �� ijͬѧΪ��ȷ����ɷ֣�ȡ������Һ����Ʋ��������ͼʵ�飺����˵����ȷ���ǣ� �� 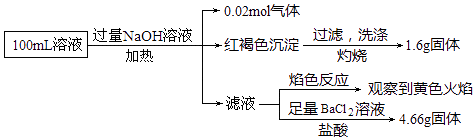
A.ԭ��Һ��c��Fe3+��=0.2molL��1
B.SO42����NH4+��Na+һ�����ڣ�CO32��һ��������
C.Ҫȷ��ԭ��Һ���Ƿ���Fe2+ �� �����Ϊȡ����ԭ��Һ���Թ��У���KSCN��Һ���ټ���������ˮ����Һ��Ѫ��ɫ������Fe2+
D.��Һ��������4�����Ӵ��ڣ�����Cl��һ�����ڣ���c��Cl������0.2molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء���������������Ӧ�õĶ�Ӧ��ϵ������ǣ� ��
A.�轺��ˮ����ǿ��������ʳƷ��ҩƷ�ĸ����
B.�����������Բ�ǿ��������θ���кͼ�
C.�������ƾ���ǿ�����ԣ�������֯���Ư��
D.�����Ǿ��������ԣ������ڹ�ҵ�ƾ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com