
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
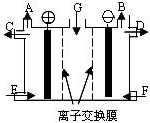 (2012?山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是( )
(2012?山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示装置中,X和Y均为石墨电极.
如图所示装置中,X和Y均为石墨电极.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:013
电解池中装饱和的Na2SO4溶液,用惰性电极和直流电进行电解,当温度不变时,溶液的:
[
]A
.浓度减小 B.浓度增大C
.浓度增大,且有晶体析出 D.浓度不变,且有晶体析出查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com