
 ��
�� ��
�� $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$ +H2O��
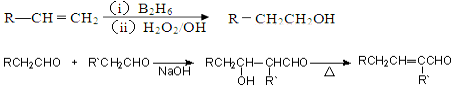
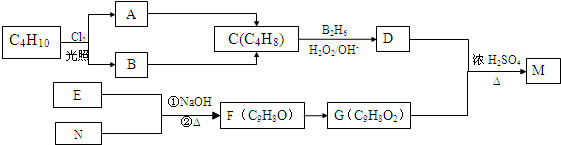
+H2O������ C�ܷ������⻯��������Ӧ����D��������Ϣ��֪��C��̼̼˫��λ�ڱ��ϣ���������ȡ����Ӧ���������ȴ������������ȴ���������ȥ��Ӧ����ͬһ��ϩ����˵����������ԭ�����������֣���������Ľṹ��ʽΪ��CH3��2CHCH3��A��B�ṹ��ʽΪ��CH3��2CHCH2Cl����CH3��2CClCH3�������������A��B������ȥ��Ӧ����C��C�ṹ��ʽΪ��CH3��2C=CH2��D�ṹ��ʽΪ��CH3��2CH2CH2OH��
FΪ�����廯���F�����Ͷ�=$\frac{9��2+2-8}{2}$=6�����������Ͷ�Ϊ4��ȩ�������Ͷ�Ϊ1��̼̼˫�����Ͷ�Ϊ1��������Ϣ��֪��F��ϩȩ���˴Ź���������ʾE��������������ԭ�ӣ���E�ṹ��ʽΪCH3CHO��N�ṹ��ʽΪ ��F�ṹ��ʽΪ
��F�ṹ��ʽΪ ������F��G�ṹ��ʽ֪��F����������Ӧ����G��G�ṹ��ʽΪ
������F��G�ṹ��ʽ֪��F����������Ӧ����G��G�ṹ��ʽΪ ��D��G����������Ӧ����M��M�ṹ��ʽΪ
��D��G����������Ӧ����M��M�ṹ��ʽΪ
��� �⣺��1��ԭ��C4H10�Ľṹ��ʽΪ��CH3��2CHCH3����������2-�����飬�ʴ�Ϊ��2-�����飻
��2��A���ȴ�����C��ϩ����A������ȥ��Ӧ����C����Ҫ��������ǿ��������ȣ��ʴ�Ϊ��ǿ��������ȣ�
��3��F�ṹ��ʽΪ ��F������������ͭ����Һ���ȷ���������Ӧ���ɱ���ϩ�ᣬ��Ӧ����ʽΪ
��F������������ͭ����Һ���ȷ���������Ӧ���ɱ���ϩ�ᣬ��Ӧ����ʽΪ��
�ʴ�Ϊ����
��4��ͨ�����Ϸ���֪��N��M�Ľṹ��ʽ�ֱ�Ϊ

�ʴ�Ϊ��

��5��D��G����M�Ļ�ѧ����ʽΪ��CH3��2CH2CH2OH+ $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$
�ʴ�Ϊ����CH3��2CH2CH2OH+ $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$
��6����G������ͬ�����ŵ�G�����з�����ͬ���칹��ṹ��ʽΪ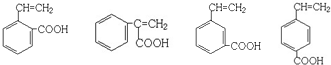 ������G����4�֣�
������G����4�֣�
�ʴ�Ϊ��4��
���� ���⿼���л���ĺϳɣ�Ϊ��Ƶ���㣬����ϰ���е���Ϣ���ϳ������й����ŵı仯���л���ӦΪ���Ĺؼ������ط������ƶ������Ŀ��飬ע���л������ʵ�Ӧ�ã���Ŀ�ѶȲ���


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��SO2ͨ��Ba��OH��2��Һ�У��а�ɫ�������ɣ��ӹ�����ϡ����������ʧ | |
| B�� | ��SO2ͨ��BaCl2��Һ�У��а�ɫ�������ɣ���ϡ����������ʧ | |
| C�� | ��SO2ͨ��Ba��OH��2��Һ�У��а�ɫ�������ɣ��ӹ�����ϡ������������ʧ | |
| D�� | ��SO2ͨ�������ữ��BaCl2��Һ�У��а�ɫ�������ɣ���ϡ������������ʧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����500mL����Һ���ɽ�0.1 mol BaCl2����500mLˮ�� | |
| B�� | Ba2+��Cl-�����ʵ���Ũ�ȶ���0.1 mol•L-1 | |
| C�� | ����ƿ��Һϡ��һ������������Һ��c��Cl-��Ϊ0.2 mol•L-1 | |
| D�� | ���Լ�ƿ��ȡ����Һ��һ�룬����ȡ��Һ�����ʵ���Ũ��Ϊ0.1 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 22.4LN2�������ӵ������������� | |
| B�� | �ڱ�״���£�11.2 L���Ȼ�̼����������Ϊ0.5NA | |
| C�� | 22g������̼���״����11.2LH2������ͬ��ԭ���� | |
| D�� | ���³�ѹ�£�5.6g������������ᷴӦת�Ƶ�������Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ�����н��п�ȼ������ȼ������ʵ��ʱ���������鴿�����ȼ | |
| B�� | ������Ũ��մ��Ƥ���ϣ�Ӧ�����ô���ˮ��ϴ��Ȼ��Ϳ��������Һ | |
| C�� | ����ϡ����ʱ����������Ͳ�м�һ�������ˮ�����ڽ�������������Ũ���� | |
| D�� | �������ὦ�����У�Ӧ������ˮ��ϴ����ϴ��գ�۾� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com