
| A | B | C | D |
 |  |  | 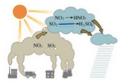 |
| 镁条的燃烧 | 人工吹制玻璃器皿 | 铜狮表面出现铜绿 | 酸雨的形成 |
| A. | A | B. | B | C. | C | D. | D |
分析 反应中存在元素的化合价变化为氧化还原反应,若不存在元素的化合价变化,则不属于氧化还原反应,以此来解答.
解答 解:A.Mg在空气中燃烧,Mg、O元素的化合价发生变化,与氧化还原反应无关,故A不选;
B.人工吹制玻璃器皿,不存在元素化合价的变化,不属于氧化还原反应,故B选;
C.铜狮表面出现铜绿,Cu、O元素的化合价发生变化,属于氧化还原反应,故C不选;
D.酸雨在形成过程中,亚硫酸被空气中的氧气氧化,S、O元素的化合价发生变化,属于氧化还原反应,故D不选.
故选B.
点评 本题考查氧化还原反应,侧重于化学与生活、生产的考查,把握发生的化学反应及反应中元素的化合价变化为解答的关键,注意从化合价角度分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用KSCN溶液检验FeCl2是否已被氧化而变质 | |
| B. | 用焰色反应鉴别NaCl和KCl | |
| C. | 用加热法除去Na2CO3中混有的NaHCO3杂质 | |
| D. | 用NaOH溶液除去MgCl2溶液中的CuCl2杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| A | 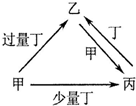 | NaOH | NaHCO3 | Na2CO3 | CO2 |
| B | C | CO | CO2 | O2 | |
| C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 | |
| D | AlCl3 | NaAlO2 | Al(OH)3 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸在反应中仅体现还原性 | |
| B. | 被氧化和被还原的物质的物质的量之比为1:1 | |
| C. | 每生成0.1molClO2转移0.2mol电子 | |
| D. | 氧化性:NaClO3<Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
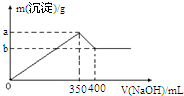 金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质.
金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含SO2的烟气可用石灰乳吸收后再排放,以减少对空气污染 | |
| B. | 汽车尾气、工业排放、建筑扬尘、垃圾焚烧等都是造成雾霾天气的主要原因 | |
| C. | 绿色化学的核心是对环境产生的污染进行治理 | |
| D. | PM2.5由于颗粒小,在空气中存在时间长,对人体健康危害大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、SO42-、OH- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | K+、Ca2+、Cl-、MnO4- | D. | Na+、CO32-、SO42-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A.海水蒸馏得到淡水 | B.中和滴定 | C.苯萃取碘水中I2,分出水层后的操作 | D.制备乙酸乙酯 |
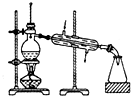 | 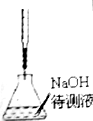 | 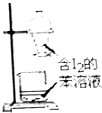 | 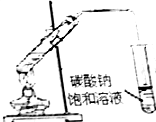 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com