
| A、影响反应速率大小的决定性因素是温度 | B、可逆反应达到化学平衡状态就是这个反应在该条件下所能达到的最大限度 | C、苯分子是一个由6个碳原子以单双键交替结合而成的六元环 | D、开发海洋资源可获得Fe、Co、K、Au、Mg、Br等金属 |


 同步轻松练习系列答案
同步轻松练习系列答案科目:高中化学 来源: 题型:
设阿伏加德罗常数为NA。。则下列说法正确的是 ( )
A.7.1g Cl2与足量NaOH溶液充分反应后,转移的电子数为O.1 NA
B.1.0L浓度为1.0 mol·L-1的一元酸溶液中含有的氢离子数为1.0 N2
C.常温下,1L 0.1 mo1.L-1的NH4NO2溶液中氮原子数小于0.2 NA
D.标准状况下,22.4L乙醛中含有的氧原子数为1.0 NA
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
依照阿伏加德罗定律,下列叙述正确的是
( ) A.同温同压下两种气体的体积之比等于摩尔质量之比。
B.同温同压下两种气体的物质的量之比等于密度之比。 C.同温同压下两种气体的摩尔质量之比等于密度之比。D.同温同体积下两种气体的物质的量之比等于压强之比。
设NA表示阿伏加德罗常数,下列说法不正确的是 ( )
A. 醋酸的摩尔质量与NA个醋酸分子的质量在数值上相等。
B.标准状况下,以任意比混和的氢气和一氧化碳气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2 NA。
C.1L1mol/LCuCl2溶液中含有的Cu2+的个数为NA。
D.25℃,1.01×105Pa时,16g臭氧所含的原子数为NA。
设NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A.用惰性电极电解500mL饱和食盐水时,若溶液的pH值变为14时,则电极上转移的电子数目为NA。
B.在标准状况下,各为1mol的二氧化硫、三氧化硫的体积均约为22.4L。
C. 在常温常压下,6g石英晶体中,含有0.4NA个硅氧共价键。
D.120g由NaHSO4和KHSO3组成的混合物中含有硫原子NA个。
标准状况下,下列混合气体的平均式量可能是50的是 ( )
A.硫化氢和二氧化硫 B.一氧化氮和氧气
C.二氧化硫和溴化氢 D.碘化氢和氯气
在一个恒容密闭容器中充入11gX气体(摩尔质量为 44g·mol-1),压强为1×105pa。如果保持温度不变,继续充入X气体,使容器内压强达到5×105pa。则此时容器内的气体X的分子数约为 ( )
A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022
由二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比为 ( )
A.29∶8∶13 B.22∶1∶14 C.13∶8∶29 D.26∶16∶57
同温、同压下,CO2 和NO的混合气体 20mL,通过足量过氧化钠后气体体积减少到10mL,则原混合气体的体积比可能是 ( )
A.1∶1 B.2∶3 C.3∶2 D.1∶4
乙炔和乙烯的混合气体完全燃烧时,所需氧气的体积是原混合气体的2.7倍,则该混合气体与足量的H2发生加成反应时,消耗H2的体积是原混合气体体积的 ( ) A.1.6倍 B.1.8倍 C.1.4倍 D.1.2倍
在一定条件下,将5体积NO、5体积NO2、6体积O2混合气体置于试管中,并将试管倒立于水槽中,充分反应后,剩余气体的体积是 ( )
A.1体积 B.2体积 C.3体积 4.4体积
19世纪,化学家对氧化锆的化学式有争议.经测定锆的相对原子质量为91,其氯化物蒸气的密度是同溶、同压下H2密度的116-117倍,试判断与氯化物价态相同的氧化锆的化学式 ( )
A.ZrO B.Zr2O C.Zr2O3 D.ZrO2
常温下,向20L真空容器中通入A mol硫化氢和 Bmol氯气(A,B均为不超过5的正整数),反应完全后,容器内气体可能达到的最大密度是 ( )
A.8.5 g·L-1 B.18.25g·L-1 C.18.5 g·L-1 D.35.5 g· L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
化学电池在通讯、交通及日常生活中有着广泛的应用。
⑴下列相关说法正确的是
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、甲烷、乙烷、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提到议事日程,其首要原因是电池外壳的金属材料需要回收
⑵目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:
2Ni(OH)2+Cd(OH)2 Cd+2NiO(OH)+2H2O
已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,下列说法正确的是:
A.以上反应是可逆反应 B.反应环境为碱性
C.电池放电时Cd作负极 D.该电池是一种二次电池
⑶在宇宙飞船和其它航天器上经常使用的氢氧燃料电池是一种新型电池,其结构如图所示:a、b两个电极均由多孔的炭块组成,通入的氢气和氧气由孔隙中逸入,并在电极表面发生反应而放电。
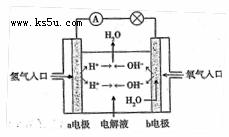
①a电极是电源的 极
②若该电池为飞行员提供了36Kg的水,则电路中通过了 mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确,并与胶体性质或用途有关的事实是 ( )
![]() ①FeCl3能用于止血;
①FeCl3能用于止血;
![]() ②硅酸胶体能用作吸附剂;
②硅酸胶体能用作吸附剂;
![]() ③明矾用于净水;
③明矾用于净水;
![]() ④在陶瓷、聚合物等材料中加入固态肢体粒子来改进材料的光学性质;
④在陶瓷、聚合物等材料中加入固态肢体粒子来改进材料的光学性质;
![]() ⑤药皂里加苯酚能消毒;
⑤药皂里加苯酚能消毒;
![]() ⑥三氧化铁溶液中加入氢氧化钠溶液出现红褐色沉淀
⑥三氧化铁溶液中加入氢氧化钠溶液出现红褐色沉淀
![]() A.①②③④ B.②④⑤⑥ C.④⑤⑥ D.③⑤⑥
A.①②③④ B.②④⑤⑥ C.④⑤⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4 (难溶盐)、Pb(MnO4)2(高锰酸铅强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1molX在该反应中应失去3.01×1023个电子。下列说法中不正确的是( )
A、若有9.8gH2SO4参加反应,则转移电子的物质的量为1mol
B、该反应的化学方程式为:5PbO2 + 2MnSO4 + 2H2SO4=== Pb(MnO4)2 + 4PbSO4 + 2H2O
C、Pb(MnO4)2既是氧化产物又是还原产物
D、X是MnSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com