
��19�֣���ɰ����Ҫ�ɷ�����״�Ĵ�����������ʯӢ��ʯ��ʯ�Ȼ���ij��ѧ��ȤС�����ɰ�з�������������������������ȷ�Ӧʵ�顣
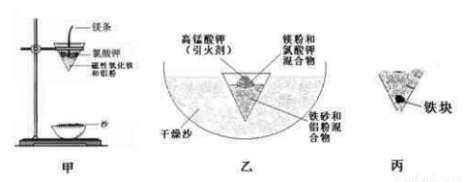
��1��ȡ������������ͼ�м�װ�ý������ȷ�Ӧ�������׳�ۡ�ȡ������Ӧ���ɵġ����顱�������ᣬ�����еμ�KSCN��Һ��������Һ��Ѫ��ɫ���������ֽ����ԭ���˿��ܻ���û��Ӧ�Ĵ����������⣬����һ��ԭ���� ��
��2��Ϊ�˿˷�ͼ�м�ȱ�ݣ�����ͼ����װ�ý������ȷ�Ӧ����Ҫ�������£�
����һ����������зŽ�һ�����ĸ���ϸɳ��
�ڽ�һ��������ɰ�����ۻ����װ��ֽ©���в�����ϸɳ�
�۽�һ������þ�ۺ�����ػ����������ȼ��ϣ�
���ٷ��������������Ӧ����ȴ����ȡ����Ӧ������飨��ͼ����
��д�����ȷ�Ӧ�Ļ�ѧ����ʽ��
ȡ������Ӧ���ɵ������������ᣬ�����еμ�KSCN��Һ����Һû�г���Ѫ��ɫ��ʵ���и���ϸɳ����Ҫ������ ��
��3���ⶨͼ���ҷ�Ӧ���õ����鴿�ȣ���������ͼ��ʾ�������������↑ʼ�����ͳ�����ȫʱ��pH�ο�19�⡣
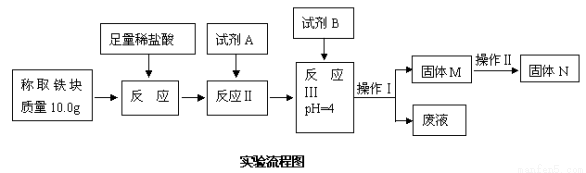
���Լ�AӦѡ�� ���Լ�BӦѡ�� ��
A��ϡ���� B�������� C��H2O2��Һ D����ˮ E��MgCO3����
�ڲ����������Ϊ �������������Ϊ ������M��ȫת��Ϊ����N�ı�־�� ��
����֪������Fe(OH)3��KSP=4.0��10-38����Ӧ�����Һ��c(Fe3+)= mol/L
�������պ�ɫ��ĩ����Ϊ14.14g���������Ĵ����� �����ֱ��ϴ�ӡ���ɺͳ�������M����������������Ĵ��ȣ���������� ���ƫ��ƫС������Ӱ�조����ԭ���� ��
��1�����ɵĺ��ȵ����ڵ��䵽����������У����汻��������ΪFe3O4 (2�֣�
��2�� 8 Al +3Fe3O4 4Al2O3 +9 Fe ��ֹ���ɵ��������� ��4�֣�
4Al2O3 +9 Fe ��ֹ���ɵ��������� ��4�֣�
��3���� C D �� �ڹ��ˣ� ϴ�ӡ� ���գ�������γ���������С��0.1g ��
��c(Fe3+)=4��10-8 mol/L��2�֣���98.98%��2�֣�ƫС���������������ں�ɹ������ֽ���ˮ��
��������
�����������1��ȡ������������ͼ�м�װ�ý������ȷ�Ӧ�������׳�ۡ�ȡ������Ӧ���ɵġ����顱�������ᣬ�����еμ�KSCN��Һ��������Һ��Ѫ��ɫ���������ֽ����ԭ���˿��ܻ���û��Ӧ�Ĵ����������⣬����һ��ԭ�������ɵĺ��ȵ����ڵ��䵽����������У����汻��������ΪFe3O4�����ȷ�Ӧ�Ļ�ѧ����ʽ��8 Al +3Fe3O4 4Al2O3 +9 Fe��ȡ������Ӧ���ɵ������������ᣬ�����еμ�KSCN��Һ����Һû�г���Ѫ��ɫ��ʵ���и���ϸɳ����Ҫ�����Ƿ�ֹ���ɵ�������������3�������з�Ӧ�����������������ܽ⣬����Һ�п��ܺ���Fe2+��Fe3+��Al3+��H+������Fe2+, Al3+������ȫʱ��Һ��pH�ܽӽ�������Һ���룬Fe3+��ȫ����ʱ��Һ��pH=3.2�����������Һ�м�����������Fe2+����ΪFe3+����������H2O2��Һ��Ȼ��ˮ������Һ��pH=4,ʹFe3+�γ�Fe(OH)3�������ٹ��˷�������������Բ����������Ϊ���ˣ������������Ϊϴ�ӡ� ���գ�����M��ȫת��Ϊ����N�ı�־��������γ���������С��0.1g��M��Fe(OH)3��N��Fe2O3�����ڳ�����Fe(OH)3��KSP=4.0��10-38����c(Fe3+)��c3(OH-)=4.0��10-38,������Һ��pH=4��c(H+)=10-4,���Ը���������ˮ�����ӻ�������10-14�ɵ�c (OH-)=10-10��c(Fe3+)=4.0��10-38��c3(OH-)=4.0��10-8mol/L���������պ�ɫ��ĩ����Ϊ14.14g��m(Fe)= (14.14g��160g/mol)��2��56g/mol=9.898g���������Ĵ�����(9.898g��10.g)��100%=98.98%�����ֱ��ϴ�ӡ���ɺͳ�������M����������������Ĵ��ȣ��������������������ں�ɹ������ֽ���ˮ��ʹ������ƫС��
4Al2O3 +9 Fe��ȡ������Ӧ���ɵ������������ᣬ�����еμ�KSCN��Һ����Һû�г���Ѫ��ɫ��ʵ���и���ϸɳ����Ҫ�����Ƿ�ֹ���ɵ�������������3�������з�Ӧ�����������������ܽ⣬����Һ�п��ܺ���Fe2+��Fe3+��Al3+��H+������Fe2+, Al3+������ȫʱ��Һ��pH�ܽӽ�������Һ���룬Fe3+��ȫ����ʱ��Һ��pH=3.2�����������Һ�м�����������Fe2+����ΪFe3+����������H2O2��Һ��Ȼ��ˮ������Һ��pH=4,ʹFe3+�γ�Fe(OH)3�������ٹ��˷�������������Բ����������Ϊ���ˣ������������Ϊϴ�ӡ� ���գ�����M��ȫת��Ϊ����N�ı�־��������γ���������С��0.1g��M��Fe(OH)3��N��Fe2O3�����ڳ�����Fe(OH)3��KSP=4.0��10-38����c(Fe3+)��c3(OH-)=4.0��10-38,������Һ��pH=4��c(H+)=10-4,���Ը���������ˮ�����ӻ�������10-14�ɵ�c (OH-)=10-10��c(Fe3+)=4.0��10-38��c3(OH-)=4.0��10-8mol/L���������պ�ɫ��ĩ����Ϊ14.14g��m(Fe)= (14.14g��160g/mol)��2��56g/mol=9.898g���������Ĵ�����(9.898g��10.g)��100%=98.98%�����ֱ��ϴ�ӡ���ɺͳ�������M����������������Ĵ��ȣ��������������������ں�ɹ������ֽ���ˮ��ʹ������ƫС��
���㣺���黯ѧʵ������������������Ӧ�����Ŀ�����ѡ�����ܽ�ƽ�������Ӧ�á����ȷ�Ӧ����ʽ����д�����ʴ��ȵļ����֪ʶ��


 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ�����������п��Ը߶���ѧģ�⣨B�����������棩 ���ͣ������
��7�֣�ú��Ϊȼ�ϣ���������������;��(��ú������̼���)��
;����C(s)��O2(g)===CO2(g) ��H����a kJ��mol��1
;����C(s)��H2O(g)===CO(g)��H2(g) ��H����b kJ��mol��1
2CO(g)��O2(g)===2CO2(g) ��H����c kJ��mol��1 2H2(g)��O2(g)===2H2O(g) ��H����d kJ��mol��1
�Իش��������⣺
��1��ȼ�յ�������ú��;����ų�������____;����ų�������(����ڡ�����С�ڡ����ڡ�)��
��2��b����ѧ��ϵʽ��______________(��a��c��d��ʾ)��
��3��������ȡˮú����Ӧ�У���Ӧ����е�������________(����ڡ�����С�ڡ����ڡ�)�����������е����������ڷ�Ӧʱ����Ӧ����Ҫ______(����ա��ų���)��������ת��Ϊ�����
��4������úͨ��;������Ϊȼ�ϵ�����__________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ�����������п��Ը߶���ѧģ�⣨A�����������棩 ���ͣ�ѡ����
�й�����ͼ��ʾԭ��ص���������ȷ����:�� ����������װ��KCl������Һ��

A��ͭƬ���������ݳ�
B��ȡ�����ź�������Ȼ����ƫת
C����Ӧ�У������е�K+������CuSO4��Һ
D����Ӧǰ��ͭƬ�������ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ�������̳�ʵ��ѧУ��һ10��ѧ����п��Ի�ѧ���������棩 ���ͣ�ѡ����
���е��뷽��ʽ����д������ǣ� ��
A��Ca��OH��2�TCa2++2OH�� B�� NaHCO3�TNa++H++CO32��
C��KHSO4�TK++H++SO42�� D��Al2��SO4��3�T2Al3++3SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ�������̳�ʵ��ѧУ��һ10��ѧ����п��Ի�ѧ���������棩 ���ͣ�ѡ����
��ͬ��ͬѹ�£�ij�����뵪��������ͬ�������Ϊ2:3����������Է�����Ϊ�� ��
A��42 B��56 C��21 D��72
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ����ʮУ����8��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ� ��
A��ͬһ����Ԫ����̬�⻯����ϵ��£���е�������
B���ǽ���������һ�����ڹ��ۼ������ӻ������п��ܴ��ڹ��ۼ�
C���Ǽ��Լ������ܴ��������ӻ������У��ɷǽ���Ԫ����ɵĻ�������һ�����������Ӽ�
D�����������ӵ�����һ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ����ʮУ����8��������ѧ�Ծ��������棩 ���ͣ�ѡ����
������ʵ�Ľ�����ȷ���ǣ� ��
A����SO2 ��SO3 �������ͨ���Ȼ�����Һ�У����ֻ�������Ϊ������BaSO4����
B��SO2ͨ����ˮ�У���ˮ��ɫ������ΪSO2��Ư����
C����Ӧ2C + SiO2  Si +2CO ������Ϊ̼�ķǽ�����ǿ�ڹ�ķǽ�����
Si +2CO ������Ϊ̼�ķǽ�����ǿ�ڹ�ķǽ�����
D����NaHCO3����Һ�еμ�NaAlO2��Һ���а�ɫ�������ɣ�����Ϊ���߷�����ȫˮ�ⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ĸ�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��˹ƥ�֣�����ʽΪC9H8O4����������֪���θ�ðҩ�����н�����ʹ���á� ����Ħ��������
A��148g B��148g/mol C��180g/mol D��146g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������к�ƽ���߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����淴Ӧ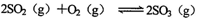 ����ƽ���ͨ��
����ƽ���ͨ��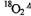 ���壬�ٴε���ƽ��ʱ
���壬�ٴε���ƽ��ʱ ������
������
A��SO2��O2�� B��SO2��SO3��
C��SO3�� D��SO2��SO3��O2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com