
【题目】下列离子方程式正确的是( )
A. 加热TiCl4浓溶液制备TiO2·xH2O:Ti4++(x+2)H2O![]() TiO2·xH2O+4H+
TiO2·xH2O+4H+
B. (NH4)2Fe(SO4)2溶液中加入少量KOH溶液:NH4+ + OH- == NH3·H2O
C. 钢铁发生吸氧腐蚀时的正极反应:O2+4H++4e-=2H2O
D. 酸性KI溶液中通入O2:4H++2I-+O2=2H2O+I2
科目:高中化学 来源: 题型:
【题目】某学生以 0.1000 mol·L-1 的 NaOH 溶液滴定 20.00mL 未知浓度的稀盐酸,滴定操作可分解为如下几步(所用的仪器已检漏且刚用蒸馏水洗净):
A.用酸式滴定管向锥形瓶里注入 20.00mL 待测稀盐酸溶液,并加入 2~3 滴酚酞;
B.用标准 NaOH 溶液润洗碱式滴定管 2~3 次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液,使管内无气泡;
D.将标准 NaOH 溶液注入碱式滴定管至刻度 0 以上 2~3cm ;
E.调节液面至 0 或 0 刻度以下,记下读数;

F.把锥形瓶放在滴定管的下面,用标准 NaOH 溶液滴定至终点并记下滴定管液面的刻度。
(1)正确操作步骤的顺序是(用序号字母填写)B_______F ;
(2)滴定达到终点的现象_________。
(3)用标准 NaOH 溶液滴定时,应将标准 NaOH 溶液注入_____(右图“甲”或“乙”)中。
(4)滴定时边滴边摇动锥形瓶,眼睛应观察_______。
(5)据下列数据计算,待测盐酸溶液的浓度为 ____mol·L-1 (计算结果保留小数点后四位)
实验编号 | 待测盐酸体积(m L) | 滴定前 NaOH 溶液的体积读数(mL) | 滴定后 NaOH 溶液 的体积读数(mL) |
1 | 20.00 | 1.20 | 23.22 |
2 | 20.00 | 2.21 | 24.21 |
3 | 20.00 | 1.50 | 23.48 |
(6)下列操作会导致测定结果偏低的是____。
A.碱式滴定管未用标准 NaOH 溶液润洗就装标准液滴定
B.读取标准液读数时,滴前仰视,滴定到终点后俯视
C.滴定前碱式滴定管尖嘴处有气泡未排除,滴定后气泡消失
D.酸式滴定管没有用待测盐酸润洗,直接装入待测盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.所有不锈钢都只含有金属元素
B.我国流通的硬币材质是金属单质
C.广东正在打捞的明代沉船上存在大量铝制餐具
D.镁合金的硬度和强度均高于纯镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与电化学腐蚀无关的是( )
A.光亮的自行车钢圈不易生锈
B.黄铜(Cu、Zn合金)制的铜锣不易产生铜绿
C.铜、铝电线一般不连接起来作导线
D.生铁比熟铁(几乎是纯铁)容易生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
①在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为__________________________。
②甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
a.CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) △H1=+49.0kJ·mol—1
CO2(g)+3H2(g) △H1=+49.0kJ·mol—1
b. ![]() △H2
△H2
已知H2(g)+ ![]() O2(g)
O2(g) ![]() H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1
则反应②的△H2=_________ kJ·mol-1。
(2)工业上一般可采用下列反应来合成甲醇:CO(g)+2H2(g)CH3OH(g),现实验室模拟该反应并进行分析,图1是该反应在不同温度下CO的转化率随时间变化的曲线。
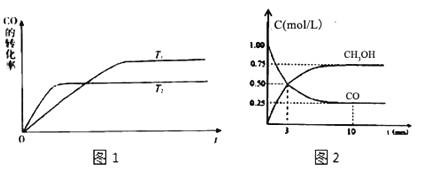
①该反应的焓变△H_____0(填“>”“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1_____K2(填“>”“<”或“=”)
③现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡,CO的平均反应速率v(CO)=_____,该反应的平衡常数为K=_____。
④恒容条件下,达到平衡后,下列措施中能使![]() 增大的有_____。
增大的有_____。
A.升高温度 B.充入He(g)
C.再充入1molCO 和3molH2 D.使用催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A(分子式为:C6H6O2)是一种有机化工原料,在空气中易被氧化。由A 合成黄樟油(E)和香料F的合成路线如下(部分反应条件已略去):
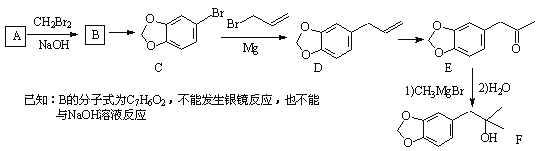
(1)写出E中含氧官能团的名称: 和 。
(2)写出反应C→D的反应类型: 。
(3)写出反应A→B的化学方程式: 。
(4)某芳香化合物是D的同分异构体,且分子中只有两种不同化学环境的氢。写出该芳香化合物的结构简式: (任写一种)。
(5)根据已有知识并结合流程中相关信息,写出以![]() 、
、![]() 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH3CH2Br ![]() CH2=CH2
CH2=CH2![]()
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com