
【题目】相同碳原子数的烷烃、烯烃、炔烃,在空气中完全燃烧生成二氧化碳和水,需要空气量的比较中正确是( )
A.烷烃最多
B.烯烃最多
C.炔烃最多
D.三者一样多
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)(Ⅰ)已知在448℃时,反应H2(g)+I2(g)2HI(g)的平衡常数 K1为49,则该温度下反应2HI(g)H2(g)+I2(g)的平衡常数K2为![]() ;反应
;反应 ![]() H2(g)+
H2(g)+ ![]() I2(g)HI(g)的平衡常数K3为 .
I2(g)HI(g)的平衡常数K3为 .
(2)(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K= .
②该反应为反应(填“吸热”或“放热”).
③能判断该反应达到化学平衡状态的依据是 .
A.容器中压强不变 B.混合气体中c(CO)不变 C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向(填“正向”或“逆向”)进行.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 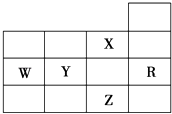
A.W元素的第一电离能小于Y元素的第一电离能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是
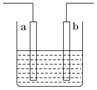
A. a、b不可能是同种材料的电极
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. 该装置可能是原电池,电解质溶液为稀盐酸
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.淀粉水解的最终产物都是氨基酸
B.淀粉和纤维素都可以作为工业上生产葡萄糖的原料
C.油脂的水解反应,都是皂化反应
D.蔗糖是高分子化合物,其水解产物能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=﹣lg[OH﹣])与pH的变化关系如图所示,则( ) 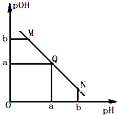
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO﹣)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某体积固定的密闭容器中加入0.3 mol A、0.1 mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:

(1)密闭容器的体积是_____L;
(2)若t1=15时,则t0~t1 s内以C物质浓度变化表示的反应速率v(C)=_______;
(3)写出反应的化学方程式:________________________;
(4)t1 s时,A的转化率为__________,此时v(A)正______v(B)逆(选填“>”、“<”或“=”);
(5)B的起始的物质的量是_____;
(6)平衡时体系内的压强为初始状态的___________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。
I.工业上通常采用电解法制氯气:观察下图,回答:

(1)若饱和食盐水中含有酚酞,通电后_____(填a或b)侧先变红。
(2)电解反应的化学方程式为_______________________。
II. 某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为_________________________________________
(2)漂白粉将在U形管中产生,其化学方程式是__________________________________。
(3)C装置的作用是_____________________。
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_________________________________。
②试判断另一个副反应(用化学方程式表示)_______________________________________。为避免此副反应的发生,可将装置作何改进_____________________________________。
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是______________。
A.食盐 B.食醋 C.烧碱 D.纯碱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com