
【题目】分类是化学学习和研究的常用方法之一。下列物质的分类正确的是 ( )
A.H2O、H2CO3、NH3都是氧化物
B.食用醋、冰红茶、加碘盐都是混合物
C.烧碱、纯碱、熟石灰都属于碱
D.液氧、氨水、铁都是常用纯净物
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种元素,已知:①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。请回答:
(1)Y的最高价氧化物对应水化物的化学式是_________________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是_________________,此液体具有的性质是______________(填写序号字母)
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼热后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1mol该气体被O2完全氧化放热98.0kJ,若2mol该气体与1molO2在此条件下发生反应,达到平衡时放出的热量是176.4kJ,则该气体的转化率为_____。
②原无色有刺激性气味的气体与含1.5molY的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】消毒剂在生产、生活中有重要的作用,常见的含氯消毒剂有NaClO2、NaClO、ClO2和Cl2。回答下列问题:
(1)NaClO2所含的化学键类型有___________。
(2)消毒剂投入水中,一段时间后与氨结合得到一种结合性氯胺(NH2C1)。NH2C1在中性或酸性条件下也是一种强杀菌消毒剂,常用于城市自来水消毒。其理由是___________(用化学方程式表示)。
(3)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。上述四种含氯消毒剂中消毒能力最强的是_____。
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。用碘量法检测ClO2处理后的自来水中ClO2浓度的实验步骤如下:
步骤I.取一定体积的水样,加入足量碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。
步骤Ⅱ.用Na2S2O3溶液滴定步骤I中所得的溶液。
已知:a.操作时,不同pH环境中粒子种类如下表所示。
pH | 2 | 7 |
粒子种类 | Cl- | ClO2- |
b.2S2O32- +I2=S4O62-+2I-。
①步骤Ⅱ中反应结束时溶液呈____(填“蓝色”或“无色”)。
②若水样的体积为1.0L,在步骤Ⅱ中消耗10mL1.0×10-3 mol·L-l Na2S2O3溶液,则该水样中c(ClO2)=____mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质X的结构简式如图所示,它常被用于制香料或作为饮料酸化剂,在医学上也有广泛用途。下列关于物质X的说法正确的是( )
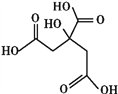
A. X的分子式为C6H7O7
B. X分子内所有原子均在同一平面内
C. 1 mol物质X最多可以和3 mol氢气发生加成反应
D. 足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体缺铁时,红细胞中血红蛋白的含量会减少,红细胞输送氧的能力也会下降,这种现象说明铁在人体具有下列哪种功能
A. 催化合成血红蛋白的反应 B. 血红蛋白的组成成分
C. 调节细胞中液体的浓度 D. 调节血浆的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Fe2O3 (s)+C(s)= CO2(g)+2Fe(s) △H=234.1kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1 则2Fe(s)+O2(g ) = Fe2O3(s) 的△H是
A.-824.4kJ·mol-1B.-627.6kJ·mol-1
C.-744.7kJ·mol-1D.-169.4kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH标准溶液滴定盐酸,以下操作导致测定结果偏低的是( )
A.滴定管用待装液润洗B.锥形瓶用待测液润洗
C.滴定结束滴定管末端有气泡D.滴定时锥形瓶中有液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
Ga和As在材料科学领域用途广泛。请回答下列问题:
(1)基态Ga原子价层电子的轨道表达式为_________;其核外电子占据最高能级的符号为___________。
(2)GaAs是优良的半导体材料,晶胞结构与金刚石相似。该晶体中不含有的化学键类型
为___________(填选项字母)。
A.σ键 B.π键 C.配位键 D.金属键
(3)Ga、N、As的合金材料是制作太阳能电池的重要原料,三种基态原子的第一电离能由小到大的顺序为________________________(用元素符号表示)。
(4)AsH3的立体构型为___________。相同压强下,AsH3的沸点低于NH3的原因为___________。
(5)LiZnAS基稀磁半导体晶胞如图所示,该晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA。则:

①与Li原子距离最近且相等的Zn原子的数目为____________。
②晶胞参数a =_____________pm(用代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com