
| A. | 0.46g | B. | 0.69g | C. | 0.92g | D. | 0.23g |
分析 将一定量的钠铝合金置于水中,合金全部溶解,得到20mL浓度为1mol/L的NaOH溶液,故溶液中溶质为氢氧化钠、偏铝酸钠,向溶液中加入lmol•L-1的盐酸滴定,至沉淀质量最大时,此时溶液中溶质为氯化钠,根据溶液中电荷守恒可知n(Na+)=n(Cl-),从而可知金属钠的物质的量,再根据m=nM计算出合金中钠的质量.
解答 解:将一定量的钠铝合金置于水中,合金全部溶解,得到20mL浓度为1mol/L的NaOH溶液,反应后溶液呈碱性,则溶液中溶质为NaOH和NaAlO2,向溶液中加入lmol•L-1的盐酸滴定,至沉淀质量最大时,此时溶液中溶质为NaCl,
根据溶液中电荷守恒可知:n(Na+)=n(Cl-)=0.04mol×1mol/L=0.04mol,根据钠元素守恒可知原合金中钠为0.4mol,
所以原合金中钠的质量为:0.04mol×23g/mol=0.92g,
故选C.
点评 本题考查混合物反应的计算,题目难度中等,根据反应实质及质量守恒得出n(Na+)=n(Cl-)是解题关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 先加BaCl2溶液过滤,再加AgNO3溶液 | |
| B. | 先加AgNO3溶液,再加稀硝酸溶液 | |
| C. | 先加足量的Ba(NO3)2溶液,过滤,再加AgNO3溶液 | |
| D. | 先加足量的BaCl2溶液,过滤,再加AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正价依次增高 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的金属性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO是弱酸,但可与NaHCO3饱和溶液反应 | |
| B. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| C. | 氯水与活性炭使红墨水褪色的原理相同 | |
| D. | 浓盐酸及浓硫酸长期暴露在空气中浓度均降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用 NaOH 溶液清洗沾在皮肤上的苯酚 | |
| B. | 用稀硝酸洗去做完银镜反应后的试管 | |
| C. | 用酸性 KMnO4除去乙烷中混有的乙烯 | |
| D. | 用酒精萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴化钾溶液跟适量氯水反应 Cl2+2Br-═Br2+2Cl- | |
| B. | 碳酸钠溶液跟足量盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| C. | 将铁粉放入稀盐酸中 Fe+2H+═Fe2++H2↑ | |
| D. | 将金属钠放入水中 Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
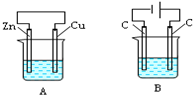 如图所示,A、B两个装置中两个烧杯分别盛有足量的CuSO4溶液:
如图所示,A、B两个装置中两个烧杯分别盛有足量的CuSO4溶液:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com