
(1)已知某混合气体的体积百分组成为80.0%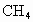 、15.0%
、15.0%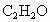 .请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
.请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
(2)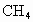 在一定条件下催化氧化可以生成
在一定条件下催化氧化可以生成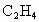 、
、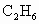 (水和其他产物忽略不计).取一定量
(水和其他产物忽略不计).取一定量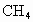 经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中
经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中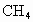 消耗了20.0%,计算混合气体中
消耗了20.0%,计算混合气体中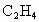 的体积百分含量.(本题计算过程中请保留3位有效数字)
的体积百分含量.(本题计算过程中请保留3位有效数字)
科目:高中化学 来源:黄冈重点作业·高二化学(下) 题型:038
(1)已知某混合气体中各成分的体积分数为CH4 80.0%、C2H4 15.0%和C2H6 5.0%.请计算0.500mol该混合气体的质量和标准状况下的密度(g·L-1).
(2)CH4在一定条件下催化氧化可以生在C2H4、C2H6(水和其他反应产物忽略不计).取一定质量的CH4经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g·L-1.已知反应中CH4消耗了20.0%,计算混合气体中C2H4的体积分数.(本题计算过程中请保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:038
(1)已知某混合气体的成分按体积分数计算是:80.0%CH4、15.0%C2H4和5.00%C2H6.请计算0.5mol该混合气体的质量和标准状况下的密度(g·L-1).
(2)CH4在一定条件下催化氧化可以生成C2H4和C2H6(水和其他产物忽略不计).取一定量CH4经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g·L-1.已知反应中CH4消耗了20%,计算混合气中C2H4的体积分数.
查看答案和解析>>
科目:高中化学 来源:高中化学同步单元练习册 全册 高二年级 题型:038
(1)已知某混合气体的体积分数为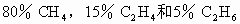 ,计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
,计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
(2)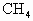 在一定条件下催化氧化可以生成
在一定条件下催化氧化可以生成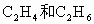 (水和其它反应产物忽略不计).取一定量
(水和其它反应产物忽略不计).取一定量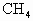 经催化氧化后得到一种混合气,它在标准状况下的密度为0.780g/L.已知反应中
经催化氧化后得到一种混合气,它在标准状况下的密度为0.780g/L.已知反应中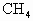 消耗了20.0%,计算混合气体中
消耗了20.0%,计算混合气体中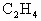 的体积分数.(计算结果保留3位有效数字)
的体积分数.(计算结果保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:058
(1)已知某混合气体的体积百分组成为80.0%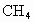 、15.0%
、15.0%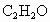 .请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
.请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
(2)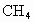 在一定条件下催化氧化可以生成
在一定条件下催化氧化可以生成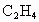 、
、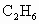 (水和其他产物忽略不计).取一定量
(水和其他产物忽略不计).取一定量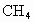 经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中
经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中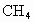 消耗了20.0%,计算混合气体中
消耗了20.0%,计算混合气体中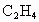 的体积百分含量.(本题计算过程中请保留3位有效数字)
的体积百分含量.(本题计算过程中请保留3位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com