
【题目】X、Y、Z、W 是原子序数依次增大的短周期主族元素, 且 X、Z 原子序数之和是 Y、W 原子序数之和的![]() 。甲、乙 、丙、丁是由这些元素组成的二元化合物, M 是某种元素对应的单质, 乙和丁的组成元素相同, 且乙是一种“绿色氧化剂”, 化合物 N 是具有漂白性的气体(常温下)。上述质物间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是:
。甲、乙 、丙、丁是由这些元素组成的二元化合物, M 是某种元素对应的单质, 乙和丁的组成元素相同, 且乙是一种“绿色氧化剂”, 化合物 N 是具有漂白性的气体(常温下)。上述质物间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是:
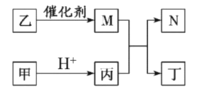
A.沸点:丁>丙,热稳定性:丁>丙
B.原子半径: r(Y) > r(Z) > r(W)
C.Z 与 X、Y、W 形成的化合物中,各元素均满足 8 电子结构
D.化合物N 与乙烯均能使溴水褪色, 且原理相同
【答案】A
【解析】
乙是一种“绿色氧化剂”,即乙为H2O2,乙和丁组成的元素相同,则丁为H2O,化合物N是具有漂白性的气体(常温下),则N为SO2,根据转化关系,M是单质,H2O2分解成O2和H2O,即M为O2,甲在酸中生成丙,丙为二元化合物,且含有S元素,即丙为H2S,四种元素原子序数依次增大,且都为短周期元素,X为H,Y为O,如果W为S,X、Z原子序数之和是Y、W原子序数之和的1/2,则Z为Na,如果Z为S,则W不符合要求。
A. 丁为H2O,丙为H2S,非金属性:O>S,则热稳定性:H2O>H2S,同时水分子间存在氢键,则沸点:H2O>H2S ,A项正确;
B. 同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,原子半径大小顺序是r(Na)>r(s)>r(O),B项错误;
C. 形成化合物分别是NaH、Na2O/Na2O2、Na2S,NaH中H最外层有2个电子,不满足8电子结构,C项错误;
D. SO2能使溴水褪色,发生SO2+Br2+H2O=2HBr+H2SO4,利用SO2的还原性,乙烯和溴水反应,发生的加成反应,原理不同,D项错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】卡莫氟G是一种抗肿瘤药,卡莫氟具有抑制病毒复制的效果.可能用于治疗感染新型冠状病毒的患者。G的一种合成路线如图所示:

已知:
①AF分子碳链中均不含环状和支链结构。
②H-N=C=O+NH3→![]()
回答下列问题:
(1)A中官能团的名称为___________。
(2)写出B和银氨溶液反应的化学方程式___________。
(3)C→D的反应类型为___________。
(4)F与5—FU反应生成卡莫氟G,5一FU的结构简式为___________,G的分子式为__________________________,
(5)F(C6H13N=C=O)的一种同系物H结构简式为C3H7N=C=O,H的同分异构体中含结构![]() ,但是不含环状结构的共有___________种(不包括立体异构),写出一种核磁共振氢谱为五组峰的同分异构体结构简式___________。
,但是不含环状结构的共有___________种(不包括立体异构),写出一种核磁共振氢谱为五组峰的同分异构体结构简式___________。
(6)DMF(N.N—二甲基甲酰胺)结构简式为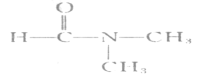 ,是一种重要的化工原料及溶剂。已知R-OH+NH3→RNH2+H2O;R—COOR’+NH3→RCONH2+R’OH。写出以CH3OH为原料制备DMF的合成路线(无机试剂任选)。____________
,是一种重要的化工原料及溶剂。已知R-OH+NH3→RNH2+H2O;R—COOR’+NH3→RCONH2+R’OH。写出以CH3OH为原料制备DMF的合成路线(无机试剂任选)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3. 84 g铜粉与一定质量浓硝酸反应,当铜完全作用时,溶液中的NO3-减少0.1mol,则所消耗硝酸的物质的量是
A.0.1 molB.0.11 molC.0.16 molD.0.22 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)书写浓硫酸与木炭在加热条件下的化学方程式为__________。
(2)试用下列各装置设计一个实验,验证上述反应所产生的各种产物。 这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):__________→__________→__________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,证明___________,B瓶溶液的作用____________,C瓶的溶液有___________现象,证明____________。
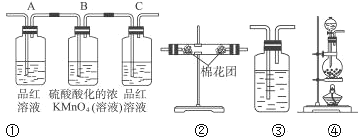
(4)书写B中的离子方程式____________。B中放置溴水不如高锰酸钾的原因____________________________。
(5)装置③中所盛溶液是__________,可验证的产物是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌—空气燃料电池有比能量高、容量大、使用寿命长等优点,可用作电动车动力电源,电池的电解质溶液为 KOH 溶液,放电时发生反应:2Zn + O2+4OH-+2H2O= 2[Zn(OH)4]2-。下列说法正确的是:
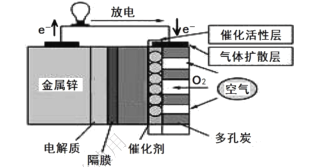
A.放电时,负极反应为 Zn-2e- = Zn2+
B.该隔膜为阳离子交换膜,允许K+通过
C.充电时,当 0.1 molO2 生成时,流经电解质溶液的电子个数约为 1.204×1022
D.采用多孔炭可提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,给空气环境造成了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )

A. 反应中NO为氧化剂,N2为氧化产物
B. 汽车尾气的主要污染成分包括CO、NO和N2
C. NO和O2必须在催化剂表面才能反应
D. 催化转化总化学方程式为2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“心得安”是质料心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):
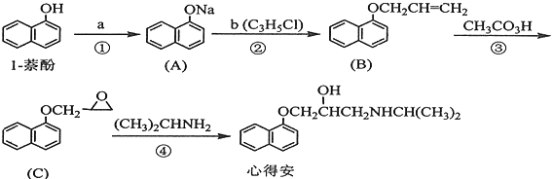
回答下列问题:
(1)试剂a是____________,试剂b的结构简式为______________,b中官能团的名称是_______________。
(2)③的反应类型是____________________。
(3)心得安的分子式为_______________-。
(4)试剂b可由丙烷经三步反应合成:
![]()
反应1的试剂与条件为_______________,反应2的化学方程式为_______________,反应3的反应类型是_______________。(其他合理答案也可)
(5)芳香化合物D是1-萘(酚)的同分异构体,其分子中有两个官能团,能发生银镜反应,D能被KMnO4酸性溶液氧化成E(C2H4O2)和芳香化合物F(C8H6O4), E和F与碳酸氢钠溶液反应均能放出CO2气体,F芳环上的一硝化产物只有一种。D的结构简式为_______________ ;由F生成一硝化产物的化学方程式为_______________,该产物的名称是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气排放出的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(1)已知:①CO燃烧热的△H1=-283.0kJ·mol-l,②N2(g)+O2(g) ![]() 2NO(g) △H2=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g)
2NO(g) △H2=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g); △H=___。
N2(g)+2CO2(g); △H=___。
(2)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生上述反应,反应过程中部分物质的浓度变化如下图所示.
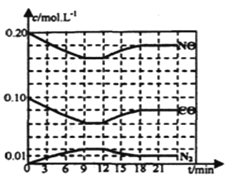
①该反应第一次达到平衡时的平衡常数为________。
②第12min时改变的条件是________。
③在第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将________移动(填“正向”、“逆向”或“不”).
(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素。
①SNCR脱硝技术中:在催化剂作用下用NH3作还原剂还原NO,其主要反应为:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0。体系温度直接影响SNCR技术的脱硝效率,如图所示。当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是________。
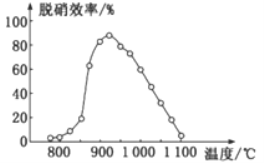
②SCR脱硝技术中则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。
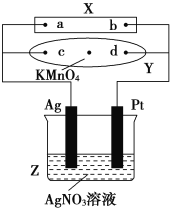
(1)电源正极为_______(填a或者b),滤纸上c点附近会变________色。
(2)电解一段时间后,产生280 mL的气体(标准状况下),此时溶液的体积为500 mL,假设溶液中还有AgNO3存在,则Z中溶液需加入________g的________可使溶液复原。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com