
��6�֣�����ͼ��ʾ�������ݻ���ͬ�����������١��ڡ��۽������µķ�Ӧ��3A��g����B��g�� 2C��g����H��0
2C��g����H��0
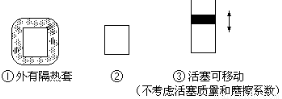
��1������ʼ�¶���ͬ���ֱ������������г���3mol A�� 1mol B����ﵽƽ��ʱ��������C���ʵİٷֺ����ɴ�С��˳��Ϊ ����������ţ�
��2����ά���¶Ȳ��䣬��ʼʱ����Ͷ��3mol A��1mol B�� ����Ͷ��3mol A��1mol B��2mol C����ﵽƽ��ʱ����������B��ת���ʢ� �ۣ��������
��3����ά�֢ڢ��������¶Ⱥ�ѹǿ��ȣ���ʼʱ�ڢ���Ͷ��3molA��1molB���ڢ���Ͷ��amol A��bmol B��cmol C����ʹ��ƽ��ʱ��������C�İٷֺ�����ȣ�������������ʼͶ�����������㣨�ú�a��b��c�Ĺ�ϵʽ�����
��6�֣�ÿ��2��)����1���ۢڢ� ��2�� �� ��3��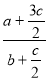 ��3
��3
��������
�����������1�����Ǻ����������Ǻ��º����������Ǻ��º�ѹ�������٢���ȣ��÷�Ӧ�Ƿ��ȷ�Ӧ�����Ԣ���ϵ���¶����ߣ����¶�����ƽ�������ƶ���ʹC���ʵİٷֺ������ͣ����Ԣ�>�٣��ڢ���ȣ��÷�Ӧ���������ʵ������ٵķ�Ӧ�����Ժ���ʱ�ڵ�ѹǿС�ڢۣ���ʹ�ڢ۴ﵽ��ͬ��״̬����Ӧ����ڵ�ѹǿ������ѹǿ��ƽ�������ƶ���ʹC���ʵİٷֺ����������Ԣ�>�ڣ��������������C���ʵİٷֺ����ɴ�С��˳��Ϊ�ۢڢ٣�
��2�����е�2molC��ȫת��ΪA��BҲ��3mol��1mol���൱�ڢ��еķ�Ӧ������ʵ����ֱ���6mol��2mol���Ǣ�������2�������ݣ�1���ķ��������ڢ��з�Ӧ������ʵ���������3molA��1molB�����ƽ��ʱ��B��ת���ʢ�>�ڣ����������ٳ���3molA��1molB����ﵽ����ƽ����ԭƽ���Ч��B��ת���ʲ��䣬��������B��ת���ʢ�>�ڣ�
��3�����º�ѹ�����£���ƽ��ʱ��������C�İٷֺ�����ȣ���ﵽ��ƽ���ǵ�Чƽ�⣬���Ԣ���Ͷ���A��B���������ʵ���֮����3:1����Cת��ΪA��B��3/2C��1/2C������A��B�����ʵ����ǣ�a+3/2C��mol����b+1/2C��mol����a+3/2C��/��b+1/2C��=3��
���㣺���鲻ͬ������ƽ����жϣ���Чƽ���Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�����и߶���ѧ�����п��Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
���ࡢ֬���͵�������ά����������������������Ӫ�����ʡ�����˵������ȷ����
A�����ۺ���ά�ؾ�����(C6H10O5)n��ʾ
B������ˮ������ղ����ܷ���������Ӧ
C��������Һ�м��뱥���������Һ������ij�������������ˮ
D��֬��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ó���������ˮ��ϴ���ú��ֺ���ɫ����ߣ��ڴ˹����в������Ļ�ѧ��Ӧ��
A��4Fe(OH)2 + 2H2O + O2 ��4Fe(OH)3
B��Fe-2e- ��Fe2+
C��2H2O + O2 + 4e-��4OH-
D��Fe-3 e- ��Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪һ�ֻ��������H2��N2�������尴�������3:1��ɣ��û�������ƽ����Է�������Ϊ
A��30 B��15 C��34 D��8.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�г������۵ġ�84������Һ������Ʒ��ʶ�������������� �ٱ�ƷΪ��ɫ��Һ���ʼ��� ��ʹ��
ʱ��ˮϡ�� �ۿɶԲ;ߡ����������������Ư��dzɫ�·���������Ч�ɷݿ�����
A��Cl2 B��SO2 C��NaClO D��KMnO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
���д�ʩ����ʵ��������������ԭ�����͵���
A�����Ƶ���ˮ�ڹ�������ɫ��dz
B���ϳ�NH3��Ӧ��Ϊ���NH3�IJ��ʣ�������Ӧ��ȡ��Խϵ��¶ȵĴ�ʩ
C����ϡ�����м�����������ˮ��������������Ũ�Ƚ���
D��ʵ�����г����ű���ʳ��ˮ�ķ�ʽ�ռ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
һ�������£����ڿ��淴ӦX(g)+3Y(g) 2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc
2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc ��c
��c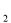 ��c
��c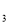 ������Ϊ�㣩������ƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol/L��0.3 mol/L��0.08 mol/L���������ж���ȷ����
������Ϊ�㣩������ƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol/L��0.3 mol/L��0.08 mol/L���������ж���ȷ����
A��c :c
:c =1:2
=1:2
B��ƽ��ʱ��Y��Z����������֮��Ϊ2:3
C��X��Y��ת�������
D��c ��ȡֵ��ΧΪ0.04 mol/L��c
��ȡֵ��ΧΪ0.04 mol/L��c ��0.14 mol/L
��0.14 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и�һ��һѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ�仯�У����������������ʵ�ֵ���
A��C��CO2 B��CO2��CO C��CuO��Cu D��H2SO4��BaSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�^����ʡ��һ��ѧ�ڵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
Ҫ��֤Mg��Fe��Cu���ֽ����Ļ��˳��ѡ�������������ʽ���ʵ��
A.Cu��FeCl2��Һ��MgCl2��Һ
B.Fe��Cu��MgCl2��Һ
C.Mg��CuO��FeSO4��Һ
D.Fe��CuSO4��Һ��MgCl2��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com