
【题目】绿色植物是空气天然的“净化器”,研究发现,1亩柳杉每天可以吸收5mol SO2 . 则1亩柳杉每天吸收的SO2的质量为( )
A.320g
B.160g
C.64g
D.32g
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】将1.0mol I2 (g)和2.4mcl H2置于某2L密闭容器中,在某一温度下发生反应H2(g)+I2(g)2HI(g)△H<0,并达平衡,12的转化率a(I2)随时间变化如图曲线Ⅱ所示 
(1)若改变反应条件,在某条件下a(I2)的变化如曲 线(I )所示,则该条件可能是:(填序号)
①恒容条件下,升高温度
②恒温条件下,缩小反应容器体积
③恒温条件下,扩大反应容器体积
④恒温、恒容条件下,加入适当催化剂
(2)该温度下此化学反应的化学平衡常数为 .
(3)在图基础上画出恒容条件下,降低温度,I2的转化率a(I2)随时间变化的曲线 .
(4)若在原平衡的基础上,保持体系温度不变,再往体系中通入1.4mol I2(g)和0.6mol HI(g),计算再次达到平衡时I2(g)的物质的量.(写出计算过程,已知最后结果保留2位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A不能使溴水褪色,0.5 mol A完全燃烧时,得到1.5 mol H2O和67.2 L CO2(标准状况)。
(1)通过计算确定A的结构简式为__________________。
(2)写出A与浓硝酸和浓硫酸的混合酸在水浴加热条件下反应生成C的化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量与我们的健康息息相关,目我国通过检测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2、和CO是其中3项中的污染物.
(1)上述3种气体直接排入空气后会引起酸雨的气体有(填化学式).
(2)处理酸雨市场采用NaClO2溶液作为吸收剂,可同时对烟气进行脱硫、脱硝,其中脱硫反应ClO2﹣+2SO32﹣2SO42﹣+Cl﹣ , 该反应的平衡常数K的表达式为;
(3)利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,写出电极A的电极方程式 , 当标况下有4.48L被处理时,通过电极B的电子数为 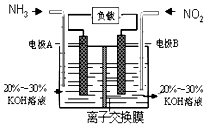
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 磷酸溶液能够导电
B. 水银属于单质
C. CuSO4·5H2O是化合物
D. “月落乌啼霜满天”——其中“霜”的形成属于升华现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,其原子序数依次增大。其中A元素原子核内只有一个质子;A与C、B与D分别同主族;B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。
请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是________(填字母)。
A.C2B2 B.DB2 C.E2 D.C2DB3
(2)D元素在元素周期表中的位置为_______________________________;化合物C2B中两种离子的半径大小关系为________ > ________(填离子符号)。_____________
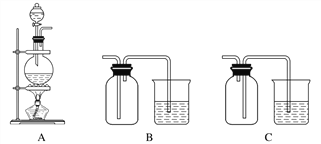
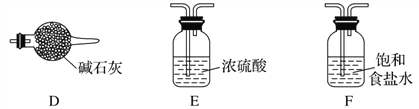
(3)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。
实验中应选用的装置为( ) → ( ) → ( ) → ( ) (按由左到右的连接顺序填写);___________
(4)试用电子式表示C2D的形成过程:___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀工业中往往产生大量的有毒废水,必须经过严格处理后才可以排放.某种含A离子(阴离子)废水在排放前的处理过程如下: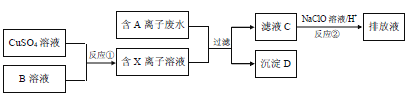
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,生成的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25gL﹣1的气体E 1.12L.
(1)E的结构式
(2)沉淀D的化学式
(3)写出沉淀D在氧气中灼烧发生的化学方程式
(4)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理
(5)反应①为制得某种元素的低价X离子,试从氧化还原反应的角度分析,是否可以用Na2SO3溶液来代替B溶液,说明理由 ,并设计实验方案证明Na2SO3溶液是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,Q、R两种元素组成的原子个数比为1:1的化合物N是中学化学中常见的有机溶剂;
⑤Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同.
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示)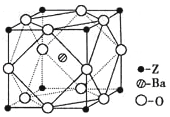
(1)化合物M的空间构型为 ,其中心原子采取 杂化;化合物N在固态时的晶体类型为
(2)R、X、Y三种元素的第一电离能由小到大的顺序为
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为 (写分子式)
(4)由R、X、Y三种元素组成的RXY﹣离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物质.该反应的离子方程式为
(5)Z原子基态时的外围电子排布式为 ;Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个Z原子等距离且最近的氧原子数为
查看答案和解析>>
科目:高中化学 来源: 题型:
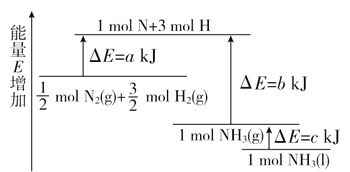
【题目】化学反应N2+3H2===2NH3的能量变化如图所示,该反应的热化学方程式是( )
A. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(a-b-c) kJ/mol
H2(g)=NH3(l) ΔH=(a-b-c) kJ/mol
B. N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a) kJ/mol
C. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a) kJ/mol
H2(g)=NH3(l) ΔH=(b+c-a) kJ/mol
D. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b) kJ/mol
H2(g)=NH3(g) ΔH=(a+b) kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com