
过渡金属催化的新型碳-碳偶联反应是近年来有机合成的研究热点之一,如:
反应①

化合物Ⅱ可由化合物Ⅲ合成:
C4H7Br CH3CHCHOHCH2
CH3CHCHOHCH2
Ⅲ Ⅳ

(1)化合物Ⅰ的分子式为________。
(2)化合物Ⅱ与Br2加成的产物的结构简式为________。
(3)化合物Ⅲ的结构简式为________。
(4)在浓硫酸存在和加热条件下,化合物Ⅳ易发生消去反应生成不含甲基的产物,该反应方程式为____________________________(注明反应条件)。因此,在碱性条件下,由Ⅳ与 反应合成Ⅱ,其反应类型为________。
反应合成Ⅱ,其反应类型为________。
(5)Ⅳ的一种同分异构体Ⅴ能发生银镜反应。Ⅴ与Ⅱ也可发生类似反应①的反应,生成化合物Ⅵ,Ⅵ的结构简式为________(写出其中一种)。
(1)C7H5OBr
(2)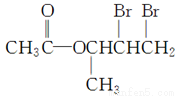
(3)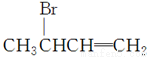
(4)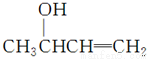
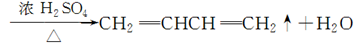 取代反应
取代反应
(5)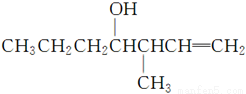
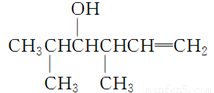 (任选一种即可)
(任选一种即可)
【解析】解答本题时,要理解反应①的机理,结合反应条件确定化合物Ⅲ和Ⅵ的结构简式。
(1)化合物Ⅰ的结构简式为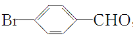 ,结合有机物中C、H、O、Br原子的成键特点可知,其分子式为C7H5OBr。
,结合有机物中C、H、O、Br原子的成键特点可知,其分子式为C7H5OBr。
(2)化合物Ⅱ中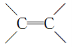 键与Br2发生加成反应,而酯基
键与Br2发生加成反应,而酯基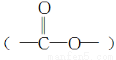 不与Br2反应,则加成产物的结构简式为
不与Br2反应,则加成产物的结构简式为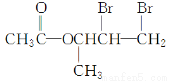 。
。
(3)化合物Ⅲ在NaOH水溶液中加热,发生水解反应生成化合物Ⅳ,递推可知Ⅲ的结构简式为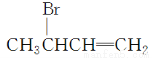 。
。
(4)化合物Ⅳ在浓硫酸存在和加热条件下,发生消去反应生成不含甲基的产物,则该产物应为CH2=CH—CH=CH2,反应的化学方程式为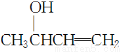
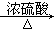 CH2=CHCH=CH2↑+H2O。在碱性条件下,
CH2=CHCH=CH2↑+H2O。在碱性条件下, 反应生成化合物Ⅱ和HCl,该反应为取代反应。
反应生成化合物Ⅱ和HCl,该反应为取代反应。
(5)Ⅴ能发生银镜反应,则Ⅴ分子中含有—CHO。含有—CHO的Ⅳ的同分异构体有CH3CH2CH2CHO、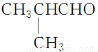 。CH3CH2CH2CHO与化合物Ⅱ发生类似反应①的反应,产物为
。CH3CH2CH2CHO与化合物Ⅱ发生类似反应①的反应,产物为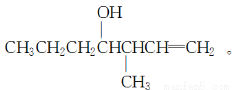
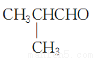 与化合物Ⅱ发生类似反应①的反应,产物为
与化合物Ⅱ发生类似反应①的反应,产物为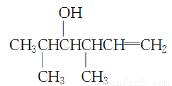 。
。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:2014年高中化学二轮创新训练上 专题7电解质溶液练习卷(解析版) 题型:填空题
环境中常见的重金属污染物有:汞、铅、锰、铬、镉。处理工业废水中含有的Cr2O72-和CrO42-,常用的方法有两种。
方法1 还原沉淀法
该法的工艺流程为 。
。
其中第①步存在平衡2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O。
Cr2O72-(橙色)+H2O。
(1)写出第①步反应的平衡常数表达式_________________________________。
(2)关于第①步反应,下列说法正确的是________。
A.通过测定溶液的pH可以判断反应是否已达平衡状态
B.该反应为氧化还原反应
C.强酸性环境,溶液的颜色为橙色
(3)第②步中,还原0.1 mol Cr2O72-,需要________mol的FeSO4·7H2O。
(4)第③步除生成Cr(OH)3外,还可能生成的沉淀为________。在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):____________________________________________________________________________。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):____________________________________________________________________________。
方法2 电解法
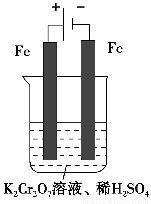
(5)实验室利用如图装置模拟电解法处理含Cr2O72-的废水,电解时阳极反应式为________,阴极反应式为________,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题4物质结构与元素周期律练习卷(解析版) 题型:选择题
下列关于指定粒子构成的叙述中,不正确的是 ( )。
A.37Cl与39K具有相同的中子数
B.第114号元素的一种核素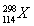 与
与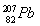 具有相同的最外层电子数
具有相同的最外层电子数
C.H3O+与OH-具有相同的质子数和电子数
D.O22-与S2-具有相同的质子数和电子数
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题2常用化学计量-物质的量练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )。
A.1 mol Al3+含有的核外电子数为3NA
B.1 mol Cl2与足量的铁反应,转移的电子数为3NA
C.室温下,10 L pH=1的硫酸溶液中含有的H+数为2NA
D.室温下,10 L pH=13的NaOH溶液中含有的OH-数为NA
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题2常用化学计量-物质的量练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列叙述错误的是( )。
A.标准状况下,11.2 L氢气中含有1 mol质子
B.12 g金刚石含有的共价键数为4NA
C.46 g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题14物质结构与性质选考练习卷(解析版) 题型:填空题
在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3=2A+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为________,含有离子键、________等化学键。
(2)生成物中含有10个电子的分子是________(写分子式),该分子的空间构型为________,中心原子的杂化方式为________。
(3)反应物中电负性最大的元素为________(填元素符号),写出其原子最外层的电子排布图:________。
(4)Al单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。

若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为________;Al晶体的密度为________(用字母表示)。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题13化学实验综合应用练习卷(解析版) 题型:填空题
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水。
Ⅰ.(1)ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得。则该反应的氧化产物与还原产物的物质的量之比是________。
Ⅱ.实验室也可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2,其流程如下:

(2)写出电解时发生反应的化学方程式:________________________________。
(3)除去ClO2中的NH3可选用的试剂是________。(填序号)
A.饱和食盐水 B.碱石灰
C.浓硫酸 D.水
(4)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100 mL水溶解后,再加3 mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol·L-1硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去V mL硫代硫酸钠溶液。

①装置中玻璃液封管的作用是______________________________________。
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式__________________________。
③滴定终点的现象是_______________________________________________。
④测得通入ClO2的质量m(ClO2)=________。(用含c、V的代数式表示)
(5)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子ClO2-。2001年我国卫生部规定,饮用水的ClO2-含量应不超过0.2 mg·L-1。若饮用水中ClO2-的含量超标,可向其中加入适量的某还原剂,该反应的氧化产物是________(填化学式),其发生反应的离子方程式为_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题12化学实验基础练习卷(解析版) 题型:选择题
欲鉴别物质的量浓度都为0.1 mol·L-1的KCl、(NH4)2SO4、NH3·H2O和H2SO4四瓶无色溶液,下列实验方案最佳的是 ( )。
A.用pH试纸鉴别
B.分别用闻气味和pH试纸鉴别
C.分别用BaCl2和NaOH溶液鉴别
D.用Ba(OH)2溶液鉴别
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 4-2资源综合利用、环境保护练习卷(解析版) 题型:选择题
下列反应不符合绿色化学基本原则的是( )
A.除硫酸厂尾气:SO2+2NH3+H2O=(NH4)2SO3
B.消除硝酸工业尾气氮氧化物的污染:2NaOH+NO2+NO=2NaNO2+H2O
C.制备CuSO4:Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.制备CuSO4:2Cu+O2 2CuO,CuO+H2SO4(稀)=CuSO4+H2O
2CuO,CuO+H2SO4(稀)=CuSO4+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com