
M是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):
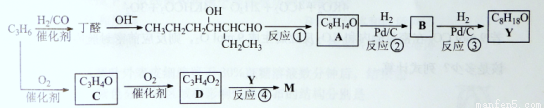
完成下列填空:
(1)反应①的反应类型是____________。反应④的反应条件是_____________。
(2)除催化氧化法外,由A得到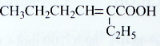 所需试剂为___________。
所需试剂为___________。
(3)已知B能发生银镜反应。由反应②、反应③说明:在该条件下,_______________。
(4)写出结构简式,C________________ D________________
(5)D与1-丁醇反应的产物与氯乙烯共聚可提高聚合物性能,写出该共聚物的结构简式。_____________
(6)写出一种满足下列条件的丁醛的同分异构体的结构简式。____________
①不含羰基 ②含有3种不同化学环境的氢原子
已知:双键碳上连有羟基的结构不稳定。
科目:高中化学 来源:2015-2016学年安徽六安新安中学、南溪中学高一期中联考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.伴有能量变化的物质变化都是化学变化
B.吸热反应一定需要加热才能发生
C.凡是放热反应的发生均无需加热
D.物质发生化学反应都伴随着能量变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高一5月月考化学试卷(解析版) 题型:选择题
在离子RO3n-中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目( )
A.A-x+n+48 B.A-x+n+24 C.A-x-n-24 D.A+x-n-24
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西南宁市高二下学期期中化学试卷(解析版) 题型:选择题
在一定条件下,Na2S溶液中存在水解平衡:S2-+H2O??HS-+OH-。下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.通入H2S,HS-浓度减小
C.升高温度, 增大
增大
D.加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西南宁市高二下学期期中化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A.电解饱和食盐水时,用铁作阳极,Cl-发生氧化反应
B.电解法精炼铜时,纯铜作阴极,Cu2+ 发生还原反应
C.电镀铜时,金属铜作阳极,电镀液可用硫酸铜溶液
D.铜锌原电池中,锌作负极,电子从锌极流向铜极
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(上海卷参考版) 题型:填空题
NaCN超标的电镀废水可用两段氧化法处理:
(1)NaCN与NaClO反应,生成NaOCN和NaCl
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为____________(选填“酸性”、“碱性”或“中性”);原因是______________________。
(1)写出第二次氧化时发生反应的离子方程式。
_______________________________________
(2)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成_________、__________和H2O。
(4)上述反应涉及到的元素中,氯原子核外电子能量最高的电子亚层是___________;H、C、N、O、Na的原子半径从小到大的顺序为_______。
(5)HCN是直线型分子,HCN是___________分子(选填“极性”或“非极性”)。HClO的电子式为___________。
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(上海卷参考版) 题型:选择题
实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示。
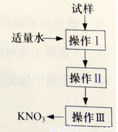
下列分析正确的是
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩。趁热过滤,除去杂质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
查看答案和解析>>
科目:高中化学 来源:2015-2016年浙江宁波效实中学高一下期中化学卷(选考)(解析版) 题型:填空题
工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业。
 (1)若采用无隔膜法电解冷的食盐水时,Cl2会与NaOH充分接触,导致产物仅是NaClO和H2。无隔膜法电解冷的食盐水相应的离子方程式为 。
(1)若采用无隔膜法电解冷的食盐水时,Cl2会与NaOH充分接触,导致产物仅是NaClO和H2。无隔膜法电解冷的食盐水相应的离子方程式为 。
 (2)
(2) 氯碱工业耗能高,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,甲,乙所用的离子膜为同一类型。
氯碱工业耗能高,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,甲,乙所用的离子膜为同一类型。
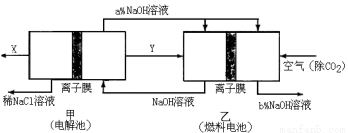
 ①甲中的离子交换膜为 (填“阳离子交换膜”或“阴离子交换膜”)。
①甲中的离子交换膜为 (填“阳离子交换膜”或“阴离子交换膜”)。
 ②经精制的饱和NaCl溶液应从图中电解池的 (填写“左” 或“右”)池注入。
②经精制的饱和NaCl溶液应从图中电解池的 (填写“左” 或“右”)池注入。
③图中X是____ __(填化学式);乙中右室的电极反应式为: _ ,图示中氢氧化钠溶液质量分数a%与b%的关系是 (填字母)。
A. a%=b% B. a%﹥b% C. a%﹤b%
查看答案和解析>>
科目:高中化学 来源:2015-2016年浙江宁波效实中学高一下期中化学卷(创)(解析版) 题型:选择题
下列图示与对应的叙述不相符的是
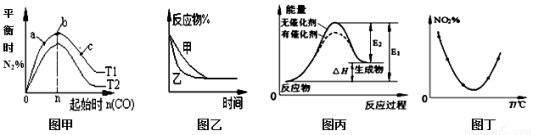
A.图甲表示反应:4CO(g)+2NO2(g) N2(g)+4CO2(g) ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
N2(g)+4CO2(g) ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
B.图乙表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(g)的影响,乙的压强比甲的压强大
3C(g)+D(g)的影响,乙的压强比甲的压强大
C.图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com