
(1)如图所示的仪器中配制溶液肯定不需要的是____________(填序号),配制上述溶液还需用到的玻璃仪器是______________(填仪器名称)。

(2)容量瓶上需标有以下6项中的_________________(填序号)
① 温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式
(3)容量瓶不_________(填序号)。
A.配制一定体积准确浓度的标准溶液 |
B.贮存溶液 |
C.测量容量瓶规格以下的任意体积的液体 |
D.准确稀释某一浓度的溶液 |
E.用来加热溶解固体溶质
(4)根据计算用托盘天平称取NaOH的质量为__________g。需用量筒量取质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为:__________mL(计算结果保留一位小数)。在配制过程中,下列操作中能引起误差偏高的有____________(填代号)。
① 未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中定容
② 定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
③ 定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④ 定容时,俯视刻度线
科目:高中化学 来源:2016-2017学年内蒙古高一上9月月考化学试卷(解析版) 题型:填空题
一定量的液态化合物XY2,在一定量 O2中恰好完全反应:XY2(l)+3O2(g)==XO2(g)+2YO2(g),其中l、g分别表示物质为液体、气体。冷却后,在标准状况下,测得生成物的体积为672mL,密度为2.56 g·L-1.
O2中恰好完全反应:XY2(l)+3O2(g)==XO2(g)+2YO2(g),其中l、g分别表示物质为液体、气体。冷却后,在标准状况下,测得生成物的体积为672mL,密度为2.56 g·L-1.
(1)反应前O2 的体积为______________。
的体积为______________。
(2)化合物XY2的摩尔质量是_____________。
(3)在XY2分子中,X、Y两元素的质量之比为3∶16,则X、Y两元素分别为___________和___________(写元素名称)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上第一次段考化学卷(解析版) 题型:选择题
下列说法不正确的是( )
A.物质的量是用来研究微观粒子的一个国际基本物理量,其单位是摩尔
B.气体的摩尔体积与温度和压强有关,压强越大,体积越大
C.若x个N (氮)原子的质量是1 g,则阿伏加德罗常数可表示为14 x mol-1
D.任何一种微观粒子,当摩尔质量以g•mol-1为单位时,其数值与这种粒子的相对分子质量或相对原子质量相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上10月月考化学试卷(解析版) 题型:选择题
100mL0.3mol·L-1的Na2SO4溶液和50mL 0.1mol·L-1的Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度为
A.0.20mol•L-1 B.0.25mol•L-1 C.0.30mol•L-1 D.0.50mol•L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上10月月考化学试卷(解析版) 题型:选择题
下列物质的水溶液能导电而本身不属于电解质的是
A.蔗糖 B.硫酸 C.二氧化碳 D.硫酸钠
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上阶段测一化学卷(解析版) 题型:选择题
把300 mL含有氯化钡和氯化钠的混合溶液分成三等份,取一份加入含x mol硫酸钾的溶液,恰好使钡离子完全沉淀;另取一份加入含y mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钠离子的物质的量浓度为( )
A.0.1(y-2x)mol/L B.10(2x-y)mol/L
C.20.10(y-x)mol/L D.10(y-2x)mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上阶段测一化学卷(解析版) 题型:选择题
已知反应:HCl + NH3 = NH4Cl(固体)如下图所示,抽去装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度。下列说法正确的是( )
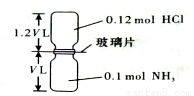
A.反应后瓶内压强是反应前的1/10 B.装置中氢元素的总质量为0.42 g
C.生成物的分子数目为0.1 NA D.反应结束后,两个集气瓶很容易分开
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第二期联考化学试卷(解析版) 题型:选择题
通过以下反应均可获取H2,下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g)ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g) =CO(g)+3H2(g)ΔH3=206.1kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)=C(s)+2H2(g)的ΔH=74.8kJ·mol–1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上10月月考化学试卷(解析版) 题型:填空题
已知:

(1)为了证明HF是弱酸,甲、乙、丙三位同学分别设计以下实验进行探究。
① 甲同学取一定体积的HF溶液,滴入2 滴紫色石蕊试液,显红色,再加入NaF 固体观察到的现象是__________________,则证明HF 为弱酸.
② 乙同学取10ml未知浓度的HF 溶液,测其pH 为a ,然后用蒸馏水稀释至1000mL .再测其pH 为b ,若要认定HF 为弱酸,则a 、b 应满足的关系是b <_____________(用含a 的代数式表示)。
③ 丙同学用pH 试纸测得室温下0.10mol.L-1的HF 溶液的pH为2 ,则认定HF为弱酸,由丙同学的实验数据可得室温下HF 的电离平衡常数约为_______________.
(2)① 己知H3BO3 与NaOH 溶液反应的离子方程式为H3BO3 +OH-=B(OH)4- ,写出硼酸的电离方程式_____________________.
② 向等浓度的H2C2O4 与H3BO3混合溶液中逐滴加入NaOH 溶液,则与OH- 作用的粒子(包括分子和离子)依次为_____________,______________,_____________。
(3)向NaHC2O4 溶液中加入少量的Na2CO3 溶液,反应的离子方程式_______________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com