
【题目】用NA表示阿伏伽德罗常数的值,下列叙述不正确的是( )
A.标准状况下,6.72LO2和N2的混合气体含有的原子数为0.6NA
B.通常状况下,8g O2和O3 的混合气体含有的分子数是0.5NA
C.常温常压下,2mol/L的100mL MgCl2溶液中,含有Cl﹣ 个数为0.4NA
D.标准状况下,11.2L H2在氧气中完全燃烧后得到的产物的分子数为0.5NA
【答案】B
【解析】A.氧气和氮气都是双原子分子,标准状况下,6.72LO2和N2的混合气体物质的量 ![]() =0.3mol,含有原子物质的量为0.6mol,含有的原子数为0.6NA,故A不符合题意;
=0.3mol,含有原子物质的量为0.6mol,含有的原子数为0.6NA,故A不符合题意;
B.氧气和臭氧摩尔质量不同,所以相同质量的氧气和臭氧物质的量不同,含有的分子数不同,故B符合题意;
C.常温常压下,2mol/L的100mL MgCl2溶液中含有氯化镁含有物质的量为2mol/L×0.1L=0.2mol,含有Cl﹣ 个数为0.2mol×2NA=0.4NA,故C不符合题意;
D.标准状况下,11.2L H2物质的量为 ![]() =0.5mol,依据2H2+O2=2H2O,可知在氧气中完全燃烧后得到的产物的分子数为0.5NA,故D不符合题意;
=0.5mol,依据2H2+O2=2H2O,可知在氧气中完全燃烧后得到的产物的分子数为0.5NA,故D不符合题意;
所以答案是:B.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】铝自然形成的氧化膜易脱落.以硫酸为电解液,分别以石墨和铝材做阴、阳极材料,经过电解处理形成的氧化铝膜,抗蚀能力强.其制备的简要流程如图.下列用来解释流程中反应的方程式不正确的是( ) 
A.碱洗目的是除去铝材表面的自然氧化膜:2OH﹣+Al2O3═2AlO2﹣+H2O
B.碱洗时铝材表面会出现气泡:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑
C.获得耐蚀铝材的电极反应为:4Al﹣12e﹣+3O2═2Al2O3
D.用稀氨水洗去耐蚀铝材表面的酸:NH3H2O+H+═NH4++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组化合物中,化学键类型完全相同的是( )
A. Mg3N2和 Na2SB. Na2O 和Na2O2C. CO2和CaOD. HCl和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义.
(1)高湿条件下,写出大气中SO2转化为HSO3﹣的方程式:
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42﹣ , 两步反应的能量变化示意图如下:
1mol H2S(g)全部氧化成SO42﹣(aq)的热化学方程式为 .
(3)二氧化硫﹣空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如下:
①质子的流动方向为(“从A到B”或“从B到A”).
②负极的电极反应式为 .
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键.SO2烟气脱除的一种工业流程如下:
①用纯碱溶液吸收SO2将其转化为HSO3﹣ , 反应的离子方程式是 .
②若石灰乳过量,将其产物再排回吸收池,其中可用于吸收SO2的物质的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠的工艺流程如图: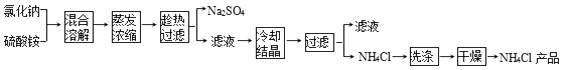
【查阅资料】
①上述流程所示物质中只有NH4Cl受热易分解:NH4Cl ![]() NH3↑+HCl↑
NH3↑+HCl↑
②氯化铵和硫酸钠的溶解度随温度变化曲线如图所示: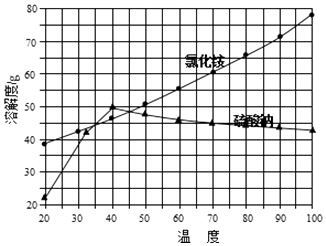
请回答下列问题:
(1)写出氯化钠和硫酸铵溶液混合得到硫酸钠晶体的化学方程式: .
(2)欲制备10.7g NH4Cl,理论上需NaCl质量为g.
(3)实验室进行蒸发结晶用到的主要仪器除铁架台、铁圈、酒精灯外,还要有 .
(4)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 .
(5)不用其它试剂,检查NH4Cl产品是否纯净的方法:
操作步骤 | 现象 | 结论 |
取少量氯化铵产品于试管底部, | 表明氯化铵产品纯净 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com