



 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ | B��ú̿ | C��ʯ�� | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������������Դ | B���������̫���� |
| C����ʹ�ú�̼��Դ | D�������Դ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH=7����Һ |
| B��c(H+) = c(OH��)����Һ |
| C����ǿ�ᡢǿ������ʵ�����Ӧ�Ƶõ���Һ |
| D���ǵ��������ˮ�õ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ʵ���������Ϊw����100% |
| B�����ʵ����ʵ���Ũ��c�� mol��L��1 |
| C����Һ��c(OH��)�� mol��L��1 |
| D��������Һ���ټ���V mLˮ��������Һ���ʵ�������������0.5w |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��10��1 | B��5��1 |
| C��1��1 | D��1��10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
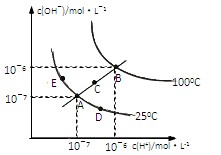
| A��ͼ�����KW��Ĺ�ϵ��B��C��A=D=E |
| B������A�㵽D�㣬�ɲ��ã��¶Ȳ�����ˮ�м����������� |
| C��������B��ʱ����pH=2��������pH=10��KOH�������Ϻ���Һ������ |
| D������A�㵽C�㣬�ɲ��ã��¶Ȳ�����ˮ�м���������NH4Cl ����ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������7 | B��С��7 | C������7 | D����ȷ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com