
【题目】下列物质溶于水中形成l mol·L-1的溶液时,导电能力最强的是
A. HCl B. H2SO4
C. CH3COOH D. CH3CH2OH
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是

A.原混合酸中NO3-物质的量为0.1 mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 molCuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
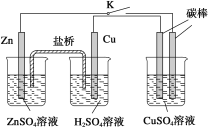
A.铜棒为正极,其电极反应式为2H++2e-→H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北魏贾思勰《齐民要术·作酢(zuò,今醋也)法》这样描述乌梅苦酒法:“乌梅去核,一升许肉,以五升苦酒渍数日,曝干,擣作(dǎo,同“捣”)作屑。欲食,辄投水中,即成醋尔。”下列有关醋的说法中正确的是
A. 醋的主要成分是非电解质 B. 醋的主要成分是强电解质
C. 醋的主要成分是弱电解质 D. 醋中只存在分子,不存在离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol·L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A.开始加入合金的质量可能为16.4g
B.标准状况下产物NO的体积为22.4L
C.生成沉淀完全时消耗NaOH溶液的体积为100mL
D.参加反应的硝酸的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含SiO2、Fe2O3等杂质)为原料冶炼铝的工艺流程如下图所示:

已知:2Na2SiO3+2NaAlO2+2H2O=Na2Al2SiO3↓+4NaOH。对上述流程中的判断正确的是
①试剂X为稀硫酸,沉淀中含有硅的化合物
②反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-
③结合质子(H+)的能力:OH->AlO2->CO32-
④Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
A. ①② B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
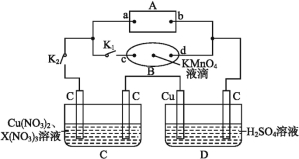
(1)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源b端为 极,通电一段时间后,滤纸d端的电极反应式是 。
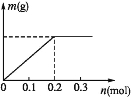
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0.1 mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是 。
(3)D装置中溶液是H2SO4溶液,则电极C端从开始至一段时间后的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:

若在反应中消耗了1 mol乙烷(反应物),则有关该反应的说法正确的是( )
A. 该反应放出251.2 kJ的热量 B. 该反应吸收251.2 kJ的热量
C. 该反应放出125.6 kJ的热量 D. 该反应吸收125.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究碳铁合金与浓硫酸在酸性条件下反应的部分产物并测定碳铁合金中铁元素的质量分数,某化学小组设计了下图所示的实验装置,并完成以下实验探究。


(1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下,Fe在浓硫酸中 ;②常温下,碳和浓硫酸不反应。
(2)装置B的作用是 。
(3)甲同学观察到装置C中有白色沉淀生成,他得出了使澄清石灰水变浑浊的气体是二氧化碳。装置A中能产生二氧化碳的化学方程式为 。
(4)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B-C之间添加装置M。装置E、F中盛放的试剂分别是酸性高锰酸钾、 。重新实验后观察到装置F中的现象是 。
(5)有些同学认为合金中铁元素的质量分数可用KMnO4溶液来测定。
(5Fe2++MnO4—+8H+==5Fe3++Mn2++4H2O)。
测定铁元素质量分数的实验步骤如下:
I.往烧瓶A中加入过量的还原剂铜使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤液B;
II.将滤液B稀释为250 mL;
III.取稀释液25.00 mL,用浓度为c mol·L—1的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL。
①步骤Ⅱ中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 ;
②滴定过程中 (填“需要”或“不需要”)加入指示剂
③铁碳合金中铁元素的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com