
【题目】下列操作、现象和结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 将等体积等浓度的HX和HY与足量的锌反应,收集产生的氢气并记录其体积 | HX收集到的氢气多 | HX是强酸 |
B | 向滴有酚酞的碳酸钠溶液中加入少量的氯化钡固体 | 红色变浅 | 碳酸钠溶液中存在水解平衡 |
C | 向反应FeCl3+3KSCN | 红色变浅 | 增大KCl的浓度,平衡逆向移动 |
D | 常温下分别测量等浓度的K2SO3和KCl溶液的pH | pH:K2SO3>KCl | 非金属性:Cl>S |
A. AB. BC. CD. D
【答案】B
【解析】
A. 将等体积等浓度的HX和HY与足量的锌反应,没说明时间,不能根据收集到的氢气量的多少判断强性强弱,故A错误;B.碳酸钠溶液中加入少量的氯化钡固体Ba2++CO32-![]() BaCO3
BaCO3![]() ,使CO32-+H2O=HCO3-+OH-平衡向左移动,滴有酚酞的溶液红色变浅,故B正确;C. 向反应FeCl3+3KSCN
,使CO32-+H2O=HCO3-+OH-平衡向左移动,滴有酚酞的溶液红色变浅,故B正确;C. 向反应FeCl3+3KSCN![]() Fe(SCN)3+3KCl中加入KCl溶液,因为KCl为强电解质,在溶液中仍然以离子形式存在,所以不影响FeCl3+3KSCN
Fe(SCN)3+3KCl中加入KCl溶液,因为KCl为强电解质,在溶液中仍然以离子形式存在,所以不影响FeCl3+3KSCN![]() Fe(SCN)3+3KCl的平衡移动,故C错误;D. 常温下分别测量等浓度的K2SO3和KCl溶液的PH,不能根据溶液pH的大小,比较元素非金属性的强弱,故D错误;答案:B。
Fe(SCN)3+3KCl的平衡移动,故C错误;D. 常温下分别测量等浓度的K2SO3和KCl溶液的PH,不能根据溶液pH的大小,比较元素非金属性的强弱,故D错误;答案:B。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验目的 | 探究Na2CO3和NaHCO3溶解度的相对大小 | 用已知浓度的NaOH溶液滴定未知浓度的稀硫酸 | 检验蔗糖与浓硫酸反应产生的CO2 | 验证镁和稀盐酸的反应的热效应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液为碱性某蓄电池的反应为Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)该蓄电池充电时,发生还原反应的物质是_______________(填选项字母)。放电时生成Fe(OH)2的质量为18 g,则外电路中转移的电子数是________________。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常在船体上镶嵌Zn块, 或与该蓄电池的__________(填“正”或“负”)极相连。该电化学防护法称为___________________。
(3)该蓄电池放电时负极电极反应式__________________,充电时阳极电极反应式_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分))对于A+2B(气)![]() nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
(1)A量的增减,平衡不移动,则A为______态。
(2)增压,平衡不移动,当n=2时,A的状态为________;当n=3时,A的状态为______。
(3)若A为固体,增大压强,C的组分含量减少,则____。
(4)升温,平衡向右移动,则该反应的逆反应为________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近段时间,全国范围内的雾霾天气严重影响了人们的身体健康,环境问题越来越受到人们的重视。汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题
请回答下列问题
(1)一氧化碳、氢气既是重要的能源,也可以催化还原NO等消除污染,还可以在一定条件下制取CH3OH。
已知:①N2(g)+O2(g)===2NO(g) △H=+180.5kJ·mol-1;
②2H2(g)+ O 2(g)===2H2O(1) △H=-571.6kJ·mol-1;
③H2O(g)===H2O(1) △H=-44kJ·mol-1。
写出H2与NO反应生成N2和水蒸气的热化学方程式:______________________。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。在密闭容器中充有10 mol CO和20molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应的△H___________0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时平衡常数K=___________,此时容器的体积为___________L。
CH3OH(g)。在密闭容器中充有10 mol CO和20molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应的△H___________0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时平衡常数K=___________,此时容器的体积为___________L。

(3)工业上采用加压条件下,在含冷却装置的吸收塔中,以去离子水为吸收剂吸收NO,得到40%的硝酸。原理如下:
2NO(g)+O2(g)![]() 2NO2(g) △H=-114 kJ/mol
2NO2(g) △H=-114 kJ/mol
3NO2(g)+H2O(l)![]() 2 HNO3(aq)+ NO(g) △H=-69 92 kJ/molo
2 HNO3(aq)+ NO(g) △H=-69 92 kJ/molo
采用降温操作的两个原因是_________________________________。
(4)利用电解原理也可以处理工厂烟气。如图为工业生产模拟装置。其中A、B为多孔电极(外接电源未画出),则A为___________极(填“正”“负”“阴”或“阳”),电极反应式为______________________。Ⅹ溶液中溶质的成分为___________(填化学式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物![]() 的叙述中,不正确的是( )
的叙述中,不正确的是( )
A. 它不能使溴水褪色,也不能使酸性KMnO4溶液褪色
B. 在FeBr3作催化剂时与Br2发生取代反应可生成三种一溴代物
C. 在一定条件下可发生加成反应
D. 一定条件下可以和浓硝酸、浓硫酸的混合物发生硝化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是

A. 整个过程中O3作催化剂
B. 反应III的方程式为O2+O===O3
C. 光化学烟雾中含甲醛、乙醛等刺激性物质
D. 反应I、反应Ⅱ均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 乙烯与苯都能使溴水褪色,但褪色原理不同
B. 1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气 5mol
C. 溴水遇到乙醛溶液出现褪色现象,是因为发生了氧化反应
D. ![]() 与
与![]() 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜[Cux(OH)yClz.mH2O]是重要的农药、医药中间体,还可用作木材防腐剂、饲料添加剂等。研究小组在实验室用某厂废铜渣(主要成分Cu、CuO,含少量Fe3O4、Ni、A12O3)制备碱式氯化铜的流程如下:
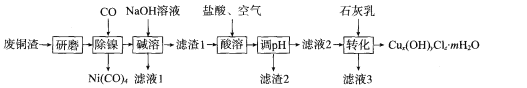
回答下列问题:
(l)“研磨”的目的为___ 。
(2)“碱溶”的目的为 __ 。
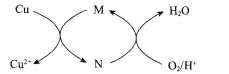
(3)“酸溶”时生成Fe3+反应的离子方程式为 ___;生成的Fe3+对Cu发生的氧化反应的催化原理如图所示。N的化学式为____。
(4)“酸溶”时温度不能过高的理由为____。
(5)若滤液2中c(Fe3+)=4×10-8 mol/L,pH=4,则Ksp[Fe(OH)3]=____。
(6)为测定Cux (OH)yClz.mH2O的组成,进行如下操作:取样品2.232 g,用适量酸溶解后配成100 mL溶液;取25. 00 mL溶液加入足量AgNO3溶液,生成0.3444 g沉淀;另取25. 00 mL溶液,用0.1600 mol.L-1的EDTA标准液滴定Cu2+(Cu2+与EDTA以物质的量之比1:1反应),滴定至终点时消耗标准液体积为30. 00 mL。
①溶解样品所用酸的化学式为 ___。
②该样品的化学式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com