������أ�K
2FeO
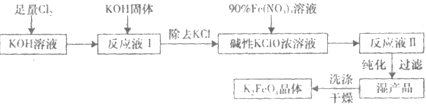
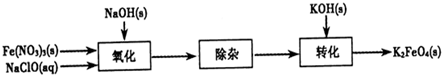
4����һ�ּ�������������������һ������Ͷ��ˮ����������ҵ�ϳ�����NaClO�������������������������£�
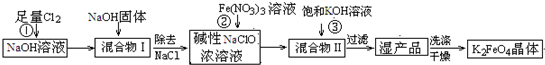
��Ҫ��ӦΪ��3NaClO+2Fe��NO
3��
3+10NaOH=2Na
2FeO
4��+3NaCl+6NaNO
3+5H
2O Na
2FeO
4+2KOH=K
2FeO
4+2NaOH��
��1��д����Ӧ�ٵ����ӷ���ʽ�� ��
��2���ӡ������II���з����K
2FeO
4���и���Ʒ ��д��ѧʽ�������Ƕ�����Ҫ�Ļ�����Ʒ������˵������һ�����ʵ���; ��
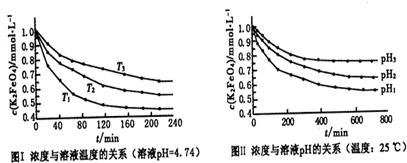
��3����Ӧ���¶ȡ�ԭ�ϵ�Ũ�Ⱥ���ȶԸ�����صIJ��ʶ���Ӱ�죮ͼ��Ϊ��ͬ���¶��£�Fe��NO
3��
3��ͬ����Ũ�ȶ�K
2FeO
4�����ʵ�Ӱ�죻ͼ��Ϊһ���¶��£�Fe��NO
3��
3����Ũ�����ʱ��NaClOŨ�ȶ�K
2FeO
4�����ʵ�Ӱ�죮

����ͼ��������ҵ����������¶�Ϊ �棬��ʱFe��NO
3��
3��NaClO������Һ�������Ũ��֮��Ϊ ��
��4��K
2FeO
4 ��ˮ��Һ����ˮ4FeO
42-+10H
2O

4Fe��OH��
3+8OH
-+3O
2�������ᴿK
2FeO
4ʱ�����ؽᾧ��ϴ�ӡ����º�ɵķ�������ϴ�Ӽ����ѡ�� ��Һ������ţ���
A��H
2O B��CH
3COONa������� C��NH
4Cl������� D��Fe��NO
3��
3�������
��5��������K
2FeO
4�ܽ���pH=4.74����Һ�У����Ƴ�c��FeO
42-��=1.0mmol?L
-1���������������ֱ�����20�桢30�桢40���60��ĺ���ˮԡ�У��ⶨc��FeO
42-���ı仯�������ͼ��ʵ���Ŀ���� ��
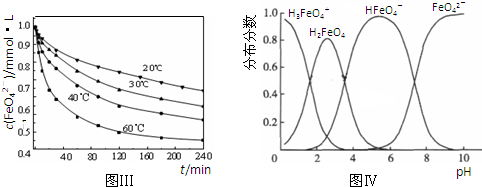
��6��FeO
42-��ˮ��Һ�еĴ�����̬��ͼ����ʾ������˵����ȷ���� ������ĸ����
A��������Һ�������α仯����Ԫ�ض���4�ִ�����̬
B����pH=10��������Һ�м�������pH=2��HFeO
4-�ķֲ�����������
C����pH=6��������Һ�м�KOH��Һ��������Ӧ�����ӷ���ʽΪ��HFeO
4-+OH
-=FeO
42-+H
2O��





 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�