
【题目】下列实验操作和现象对应的结论错误的是
选项 | 实验操作和现象 | 结论 |
A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO42- |
B | 物质的量之比为2:3的稀硝酸和稀硫酸
| 反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO |
C | 向1mL浓度均为0.05mol·L-1NaCl、NaI的混合溶液中滴加2滴0.01mol·L-1AgNO3溶液,振荡,沉淀是黄色 | Ksp(AgCl)<Ksp(AgI) |
D | 室温下,用pH试纸测得0.1mol·L-1 NaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
A. A B. B C. C D. D
【答案】C
【解析】A,向溶液X中滴加BaCl2溶液,有白色沉淀生成,此沉淀有多种可能:氯化银、碳酸钡和硫酸钡等,溶液X中可能含有Ag+、CO32-、SO42-,所以A正确。B,物质的量之比为2:3的稀硝酸和稀硫酸与过量的铜反应,恰好发生3Cu+2NO3-+8H+=3Cu2++2NO+4H2O, 反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO,所以B正确。C,向1mL浓度均为0.05mol·L-1NaCl、NaI的混合溶液中滴加2滴0.01mol·L-1AgNO3溶液,显然硝酸银溶液是很少的,在这种情况下得到黄色沉淀证明有AgI生成,所以AgI的溶度积更小,故C是错误的。D,HSO3-在溶液既能发生电离,又能发生水解,其电离出H+使溶液显碱性,而其水解会使溶液显碱性,溶液的酸碱性由两种作用的相对大小决定。室温下,用pH试纸测得0.1mol·L-1 NaHSO3溶液的pH约为5,说明HSO3-的电离程度大于其水解程度,所以D正确。


科目:高中化学 来源: 题型:
【题目】(1)用系统命名法命名CH3CH(CH3)CH=CH2 ___________________。
(2)“金刚烷”,它可以看做是由四个等同的六元环组成的空间构型。
![]()
请判断:
①一溴代物有________种。
②由氯原子取代金刚烷亚甲基(—CH2—)上的氢原子所形成的二氯代物共有_________种。
(3)写出分子式为C4H6,且能使溴水因发生反应而褪色的链烃的结构简式:____________、____________、____________
(4)某有机物,它的相对分子质量为88。将8.8g该含氧有机物充分燃烧后的产物通过浓硫酸后增重7.2g,再通过足量的澄清石灰水后,有40g白色沉淀生成。求:
① 该含氧有机物的分子式_______________;
② 该含氧有机物有多种同分异构体,写出其中能水解的同分异构体的结构简式___________、____________、___________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积恒定的密闭容器中进行反应A(s)+2B(g) ![]() C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
①混合气体的密度不变 ②容器内气体的压强不变 ③混合气体的总物质的量不变 ④B的物质的量浓度不变 ⑤v正(C)=v逆(D) ⑥容器内物质A的质量 ⑦ v正(B)=v逆(C) ⑧n(B):n(C):n(D)=2:1:1
A. ①④⑤⑥ B. ②③⑥⑦⑧ C. ②④⑤⑥⑧ D. 只有④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )

A. a和b都属于芳香族化合物
B. a和c分子中所有碳原子均处于同一平面上
C. a、b和c均能使酸性KMnO4溶液褪色
D. b和c均能与新制的Cu(OH)2反应生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂.工业上通常用自然界分布最广的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:
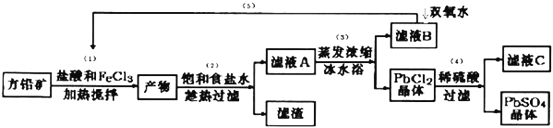
已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5.
②PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的pH值分别为1.9和7.
(I)流程中加入盐酸可以控制溶液的pH<1.9,主要目的是 _____________________,反应过程中可观察到淡黄色沉淀,则步骤(1)对应的主要反应的离子方程式为 ____________________________;
(II)步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是___________(请用平衡移动原理解释)
(III)上述流程中可循环利用的物质有___________;
(Ⅵ)步骤(4)中反应的离子方程式为_____________________.对滤液C中氯离子的测定可中和后采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl,利用Ag+与CrO42-生成砖红色沉淀,指示到达滴定终点。选用K2CrO4溶液的最好浓度等于 _____________mol·L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(Ⅴ)PbO2与MnO2性质相似,请写出PbO2与浓盐酸加热条件下反应的离子方程式______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5]有机化学基础:有机物丙(C13H18O2)是一种香料.其可由甲和乙在浓硫酸催化作用和加热条件下合成:
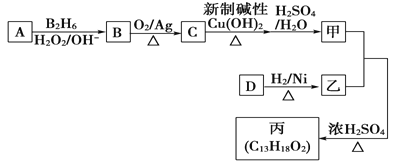
已知以下信息.:
①甲的相对分子质量为88,它的核磁共振氢谱显示有3组峰;
②乙为香醇的同系物.香醇的结构简式为: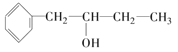
③![]()
回答下列问题:
(1)A的名称为____________。
(2)B的分子式为______________。
(3)C与新制碱性Cu(OH)2反应的化学方程式为____________。
(4)丙中有两个甲基.在一定条件下,1 mol D可以和2 mol H2反应生成乙.D可以发生银镜反应.则D 的结构简式为____________。
(5)甲与乙反应的化学方程式为______________,该反应类型为_________________:
(6)甲的同分异构体中含有“COO”结构的共有_____________种(不包含甲),其中核磁共振氢谱为3组 峰。且峰面积之比为6:1:1的为______________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 镀层破损后,白铁皮(镀锌铁板)比马口铁(镀锡铁板)更耐腐蚀
B. 埋在潮湿地下的铁管道比地上的铁管道更耐腐蚀
C. 钢铁发生析氢腐蚀时,正极上发生的电极反应式为:Fe-e-= Fe3+
D. 在钢铁表面涂上一层油漆,不能达到防止钢铁锈蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NF3分子中的中心原子采取sp3杂化,下列有关叙述正确的是( )
A. NF3分子的空间构型为三角锥形
B. NF3分子的空间构型为平面三角形
C. NF3分子的N—F键夹角与CH4分子中的C—H键的夹角相等
D. NF3分子是非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com