
| A. | 工业制金属钠:电解饱和食盐水 | |
| B. | 工业炼铁:需要用到的原料有铁矿石、一氧化碳、空气和石灰石 | |
| C. | 冶炼镁:将六水合氯化镁晶体在一定条件下加热得到无水氯化镁,电解熔融氯化镁,可以得到金属镁 | |
| D. | 生物炼铜法:利用某种能耐受铜盐毒性的细菌,这种细菌利用空气中的填氧气氧化硫化铜矿石,把不溶性的硫化铜直接转化为单质铜 |
分析 A、工业电解饱和食盐水生成NaOH、氢气、氯气,电解熔融的氯化钠制取金属钠;
B、工业炼铁原料中应有石灰石不是生石灰,工业炼铁高炉中发生的主要反应有:在高温下,焦炭跟氧气反应生成二氧化碳;二氧化碳被焦炭还原成一氧化碳;一氧化碳再跟铁矿石中的氧化物反应,生成铁,石灰石作用是除渣;
C、从海水中提取镁,可经过海水浓缩、加碱沉淀、过滤、酸溶、结晶及脱水等步骤得.到无水氯化镁,最后电解熔融的氯化镁得到金属镁;
D、微生物法是采用某些细菌能用空气中的氧气氧化硫化铜矿石.
解答 解:A、工业电解饱和食盐水生成NaOH、氢气、氯气,电解熔融的氯化钠可得到钠和氯气,故A错误;
B、工业炼铁:需要用到的原料有铁矿石、焦炭、空气和石灰石,焦炭的作用:提供热量、生成一氧化碳;一氧化碳再跟铁矿石中的氧化物反应,生成铁,石灰石在高温条件下分解能生成氧化钙和二氧化碳,氧化钙能和铁矿石中的杂质二氧化硅反应生成硅酸钙,从而除去二氧化硅,故B错误;
C、海水中含有大量镁元素,可以通过多步转化得到六水合氯化镁晶体,氯化镁易水解生成氢氧化镁和氯化氢,且氯化氢易挥发,导致直接加热带结晶水的晶体时得不到氯化镁,为防止氯化镁水解,需要将带结晶水的氯化镁在氯化氢氛围中加热,得到无水氯化镁,采用电解熔融氯化镁的方法冶炼镁,故C正确;
D、利用生物炼铜法把不溶性的硫化铜氧化,硫从负二价被氧化成正六价,最后转化成可溶的硫酸铜,成本低,污染小,反应条件十分简单,故D错误.
故选C.
点评 本题考查了金属的冶炼与工业制取浓硫酸,熟悉工业冶炼金属原理、可逆反应特点是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 容器内压强不随时间的变化而变化 | B. | X的消耗速率与Z的消耗速率相等 | ||
| C. | X、Y、Z、W的浓度相等 | D. | 总质量保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在容量瓶中定容时,俯视刻度线 | |
| B. | 用量筒量取浓盐酸时,俯视刻度线 | |
| C. | 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 | |
| D. | 定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
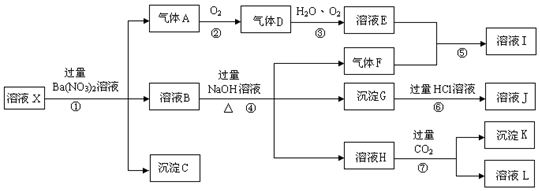
 ,实验中,可以观察到反应②的现象是:无色气体变为红棕色.
,实验中,可以观察到反应②的现象是:无色气体变为红棕色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验溶液中是否含有Fe2+时,所用KMnO4溶液用硫酸酸化 | |
| B. | 检验溶液中是否含有Br-时,所用AgNO3溶液用盐酸酸化 | |
| C. | 检验溶液中是否含有SO32-时,所用BaCl2溶液用硝酸酸化 | |
| D. | 检验溶液中是否含有SO42-时,所用BaCl2溶液用硝酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在任何条件下,纯水都呈中性 | |
| B. | 在任何条件下,纯水的pH=7 | |
| C. | 在95℃时,纯水中 c(H+)<l0-7mol/L | |
| D. | 向纯水中加入少量 NaOH固体,水的电离逆向移动,c(OH-)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
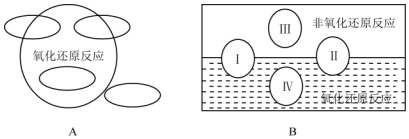 氧化还原是常见的反应类型,根据信息回答以下问题:
氧化还原是常见的反应类型,根据信息回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com