
【题目】下列原理和定律中,可用于判断化学平衡移动方向的是
A.盖斯定律B.阿伏加德罗定律C.勒夏特列原理D.质量守恒定律
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)通过火法冶金炼出的铜是粗铜,含杂质多,必须进行电解精炼。请在下面方框中画出电解精炼铜的装置______。

(2)水解反应在生产生活中有很多应用。有些盐水解程度很大,可以用于无机化合物的制备,如可以用TiCl4与H2O反应,生成TiO2·xH2O,制备时加入大量的水,同时加热。请结合化学用语和必要的文字解释“加热”的作用:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是理想的清洁能源,资源丰富。以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下:

(1)过程I :2Fe3O4(s)![]() 6FeO(s)+O2(g) △H=+313.2 kJ/mol
6FeO(s)+O2(g) △H=+313.2 kJ/mol
①过程I需要将O2不断分离出去,目的是______________。
②一定温度下,在容积可变的密闭容器中,该反应已达到平衡。下列说法正确的是____(填字母标号) 。
a.容器内气体密度和相对分子质量都不再改变
b.升高温度,容器内气体密度变大
c.向容器中通入N2,Fe3O4 转化率不变
d.缩小容器容积,O2(g)浓度变大
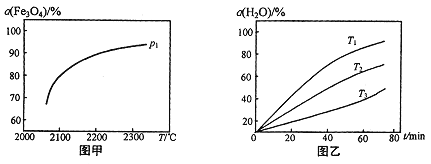
③在压强p1下,Fe3O4的平衡转化率随温度变化的曲线如图甲所示。若将压强由p1增大到p2在图甲中画出p2的α(Fe3O4)~T 曲线示意图。___________
(2)已知H2的燃烧热是285.8kJ/mol,则液态水通过过程II转化的热化学方程式为______。
(3)其他条件不变时,过程II在不同温度下,H2O的转化率随时间的变化α(H2O)~t曲线如图乙所示,温度T1、T2、T3由大到小的关系是_________,判断依据是_________。
(4)科研人员研制出透氧膜(OTM),它允许电子和O2-同时透过,可实现水连续分解制H2,工作时CO、H2O分别在透氧膜的两侧反应。工作原理如图所示:
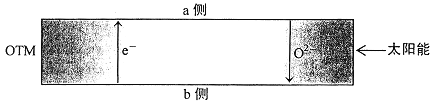
CO 在________侧反应(填“a”或“b”),另一侧的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是
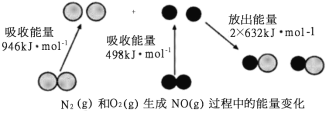
A. 1mol N2(g)和1mol O2(g)完全反应放出的能量为180kJ
B. 通常情况下,N2(g)和O2(g)混合能直接生成NO
C. 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量
D. NO是一种红棕色的气体,能与水反应生成硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置干容积为2L的密用容器中发生如下反应:4A(g)+B(g)![]() 2C (g),反皮进行到4s末,测得A、B、C的物质的量分别为0.5mol、0.4mol、0.2mol。则用反应物B表示该反应的速率为
2C (g),反皮进行到4s末,测得A、B、C的物质的量分别为0.5mol、0.4mol、0.2mol。则用反应物B表示该反应的速率为
A. 0.025mol·L-1·s-1c. B. 0.0125 mol·L-1·s-1
C. 0.05 mol·L-1·s-1 D. 0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中,由CO2和H2合成甲醇,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);

(1)下列说法正确的是_____________________(填序号);
①温度为T1时,从反应平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应为放热反应
③处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(2)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应A2 (g)+B2 (g)![]() 2C (g)达到了化学平衡状态,经测得平衡时c (A2)=0.5 mol·L-1,c (B2)=0.1 mol·L-1,c (C)=1.6 mol·L-1,若A2、B2、C的起始浓度分别以a mol·L-1,b mol·L-1,c mol·L-1表示,请填写下列空白。
2C (g)达到了化学平衡状态,经测得平衡时c (A2)=0.5 mol·L-1,c (B2)=0.1 mol·L-1,c (C)=1.6 mol·L-1,若A2、B2、C的起始浓度分别以a mol·L-1,b mol·L-1,c mol·L-1表示,请填写下列空白。
(1)a、b应满足的关系是_____________________。
(2)a的取值范围是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸燃料电池以Ca(HSO2)2固体为电解质传递H+,其基本结构如图所示,电池总反应可表示为:2H2+O2=2H2O,下列有关说法错误的是
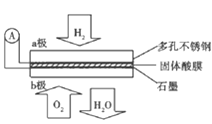
A.电子通过外电路从a极流向b极
B.b极上的电极反应式为:O2+4H+=+4e+=2H2O
C每转移0.4mol电子,生成3.6g水
D.H+由b极通过固体酸电解质传递到a极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中化学键被破坏的是
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水⑤MgCl2溶解于水 ⑥NaCl熔化
A. 全部 B. ②③④⑤⑥ C. ④⑤⑥ D. ⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com