
��ҵ������Ĺ��������÷�Ӧ2SO2��g����O2��g�� 2SO3��g������H<0����SO2ת��ΪSO3��β��SO2����NaOH��Һ�������ա���ش��������⣺
2SO3��g������H<0����SO2ת��ΪSO3��β��SO2����NaOH��Һ�������ա���ش��������⣺
��1��һ�������£���һ���������ܱ������г���2 mol SO2��1mol O2������Ӧ��������˵����ȷ���� ��
A������Ӧ����v (SO2) ��v (SO3)�������˵���ÿ��淴Ӧ�Ѵﵽƽ��״̬
B�������¶Ⱥ�����������䣬����2 mol N2����ѧ��Ӧ���ʼӿ�
C��ƽ��������Ӧ��Ũ�ȣ���ƽ��һ�����ƣ�����Ӧ���ת����һ��������
D��ƽ����ƶ�����ѹ�����壬ƽ��ʱSO2��O2�İٷֺ�����С��SO3�İٷֺ�������
E��ƽ��������¶ȣ�ƽ�ⳣ��K����
F�������¶Ⱥ�����������䣬ƽ����ٳ���2molSO3���ٴ�ƽ��ʱ�����Ũ�Ⱦ���ԭƽ��ʱ��Ũ�ȴ�
��2����һ������SO2��g����O2��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У��ڲ�ͬ�¶��½��з�Ӧ�õ����±��е��������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
��1��D F����2���� 0.2 mol�� L-1�� min-1�� 0.2 mol �� >�� 90��
��3���� 2��105 �� �� c(HSO3-)+2c(H2SO3) ������ ���� ��4��B��C = D��A ��
���������������1��A��û����ȷv����v������Ӧ����v (SO2) ��v (SO3)������˵���ÿ��淴Ӧ�Ѵﵽƽ��״̬������B�������¶Ⱥ�����������䣬����2 mol N2��SO2��SO3��O2Ũ�Ȳ��䣬��ѧ��Ӧ���ʲ��䣬����C��ƽ��������Ӧ��Ũ�ȣ���ƽ��һ�����ƣ�������Ӧ���ת���ʲ�һ����������D���÷�Ӧ����Ϊ���������С�ķ�Ӧ��ƽ����ƶ�����ѹ�����壬ƽ�������ƶ���ƽ��ʱSO2��O2�İٷֺ�����С��SO3�İٷֺ���������ȷ��E���÷�ӦΪ���ȷ�Ӧ��ƽ��������¶ȣ�ƽ�������ƶ���ƽ�ⳣ��K��С������F�������¶Ⱥ�����������䣬ƽ����ٳ���2molSO3��ƽ�������ƶ����ٴ�ƽ��ʱ�����Ũ�Ⱦ���ԭƽ��ʱ��Ũ�ȴ���ȷ��ѡDF����2���ٸ���������ݷ�����ʵ��1�ӿ�ʼ����Ӧ�ﵽ��ѧƽ��ʱO2�����ʵ����仯Ϊ1.2mol�����ݷ�Ӧ����ʽȷ��SO2�����ʵ����仯Ϊ2.4mol�����ݹ�ʽv=��n/��tV���㣬v��SO2����ʾ�ķ�Ӧ����Ϊ0.2 mol�� L-1�� min-1������������ݷ�����ʵ��2�ӿ�ʼ����Ӧ�ﵽ��ѧƽ��ʱSO2�����ʵ����仯Ϊ3.6mol�����ݷ�Ӧ����ʽȷ��O2�����ʵ����仯Ϊ1.8mol����ƽ��ʱO2�����ʵ���Ϊ0.2mol������y��0.2mol���ڸ���������ݷ������¶���T1��ΪT2,ƽ�������ƶ����÷�ӦΪ���ȷ�Ӧ�������¶ȶԻ�ѧƽ���Ӱ������жϣ��ı������Ϊ���£���T1>T2 , ����������ݷ�����ʵ��2�ӿ�ʼ����Ӧ�ﵽ��ѧƽ��ʱSO2�����ʵ����仯Ϊ3.6mol�����ݷ�Ӧ����ʽȷ��O2�����ʵ����仯Ϊ1.8mol����ʵ��2�д�ƽ��ʱ O2��ת����Ϊ90������3���ٳ�����0.1 mol/L Na2SO3��Һ��c(Na+)=0.2mol/L��ʵ��ⶨ��pHԼΪ8��c(OH��)=10��6 mol/L������Һ��c(Na+)�� c(OH��)֮��Ϊ2��105���� ���������غ㣬����Һ��c(OH-)= c(H+)+c(HSO3-)+2c(H2SO3)���� ������0.1 mol/L Na2SO3��Һ����ˮ��ƽ�⣺SO32- + H2O  HSO3- + OH-,�������Һ�м�������NaOH����ʱ��������Ũ������ƽ�������ƶ���c(SO32��)�����¶Ȳ��䣬ˮ�����ӻ�Kw���䣻��4������������ʵ���Ϊ1mol��A�����ݻ�ѧ����ʽ2SO2+Na2CO3+H2O=2NaHSO3 +CO2�жϣ�1molNa2CO3�������2molSO2��B�� ���ݻ�ѧ����ʽBa(NO3)2 +3SO2+2H2O=BaSO4+2H2SO 4�жϣ�1molBa(NO3)2 �������3molSO2��C�����ݻ�ѧ����ʽ2Na2S+SO2 +2H2O=3S+4NaOH��SO2 +NaOH=NaHSO3�жϣ�1molNa2S�������2.5molSO2��D�����ݵ����غ��жϣ�1molKMnO4�������2.5molSO2���������������ɶൽ�ٵ�˳����B��C = D��A ��
HSO3- + OH-,�������Һ�м�������NaOH����ʱ��������Ũ������ƽ�������ƶ���c(SO32��)�����¶Ȳ��䣬ˮ�����ӻ�Kw���䣻��4������������ʵ���Ϊ1mol��A�����ݻ�ѧ����ʽ2SO2+Na2CO3+H2O=2NaHSO3 +CO2�жϣ�1molNa2CO3�������2molSO2��B�� ���ݻ�ѧ����ʽBa(NO3)2 +3SO2+2H2O=BaSO4+2H2SO 4�жϣ�1molBa(NO3)2 �������3molSO2��C�����ݻ�ѧ����ʽ2Na2S+SO2 +2H2O=3S+4NaOH��SO2 +NaOH=NaHSO3�жϣ�1molNa2S�������2.5molSO2��D�����ݵ����غ��жϣ�1molKMnO4�������2.5molSO2���������������ɶൽ�ٵ�˳����B��C = D��A ��
���㣺���黯ѧ��Ӧ���ʺͻ�ѧƽ�⡢�������Һ�����ݻ�ѧ����ʽ���㡣


 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ�ص��⻯����������ڹ�ҵ�������������ж��й㷺Ӧ�ã��ش��������⣺
��1����Ԫ��ԭ�ӵ�L�������Ϊ ��
��2��NH3��NaClO��Ӧ�ɵõ��£�N2H4�����÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3���¿���Ϊ�����������ȼ�ϣ���������N2O4��Ӧ����N2��ˮ������
��֪����N2(g)+2O2(g)= N2O4(1) ��H1= -195kJ��mol-1
��N2H4(1) + O2(g)= N2(g) + 2H2O ��H2= -534��2kJ��mol-1
д���º�N2H4��Ӧ���Ȼ�ѧ����ʽ ��
��3����һ����ȼ�ϵ����һ�ּ��Ե�أ��õ�طŵ�ʱ�������ķ�ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�輰�仯����������ִ������ķ�չ��������ס���ش������й����⣺
(1)��ԭ�ӵĽṹʾ��ͼ��________��
(2)������Ʒ���豸���õIJ������ڹ����ε���________��
�ٳ�����Ͽˮ���ӡ���ʯӢ���ά�����մ�����
����ͨ�������ݹ�̫���ܵ��
| A���٢ڢ� | B���ۢܢ� | C���ڢۢ� | D���٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����ͼ��ʾװ���ռ�����4�����壨ͼ����ƿ��λ�ò��ñ仯��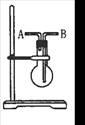
��NO����Cl2����NH3����SO2 ��д��ţ�
��1������ƿ�Ǹ���ģ�����B�ڽ����ռ���������________��
��2������ƿ�Ǹ���ģ�����A�ڽ��������ռ���������_______��
��3������ƿ����ˮ�����ռ���������________����ʱ������________���롣
��4��������ƿ��װ��Ũ����ʹ����������ô�װ���������������_____ ___����ʱ������________�ڽ��롣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ӻ�����AB2�����������ӵĵ��Ӳ�ṹ��ͬ��1 mol AB2�к�54 mol���ӣ��������з�Ӧ��
��H2��B2 C
C
��B2��X��Y��AB2��H2O
��Y��C��AB2��Z��Z��Ư�����á�
�������������ش��������⣺
��1��д���������ʵĻ�ѧʽ��AB2__________��X________��Y________��Z________��
��2���õ���ʽ��ʾAB2���γɹ��̣�_____________________________________________��
��3��д����Ӧ�ڵĻ�ѧ����ʽ��______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���������ƣ�Na2S2O5��������ʳƷƯ�������Ʊ������������£�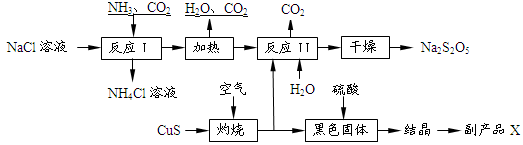
��֪����Ӧ�����2NaHSO3 Na2S2O5��H2O�ȶಽ��Ӧ��
Na2S2O5��H2O�ȶಽ��Ӧ��
��1����ӦI�Ļ�ѧ����ʽΪ�� ��
��2�������ա�ʱ������Ӧ�Ļ�ѧ����ʽ�� ��
��3����֪Na2S2O5��ϡ���ᷴӦ�ų�SO2�������ӷ���ʽΪ�� ��
��4������ƷX�Ļ�ѧʽ�� ��
��5��Ϊ�˼��ٲ�ƷNa2S2O5�����ʺ���������Ʒ�Ӧ�����������������ʵ���֮��ԼΪ �������Ʒ�к���̼�������������Լ��� �����ţ�
�����Ը�����أ���Ʒ����Һ���۳���ʯ��ˮ���ܱ���̼��������Һ����NaOH����ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ú��һ�ֳ��õ�ȼ�ϡ�����úȼ�ղ����ķ����к���SO2��NO2��NO�ȶ����к�������̳�����Ի��������Ⱦ�������Ҫ��ú���мӹ�����ȼ�գ��������������ŷš�
��1����úֱ�ӽ���ȼ�գ���ɻ�����Ⱦ����Ҫԭ��֮һ���γ����������ꡣ
��д���й�����ת��Ϊ����Ļ�ѧ����ʽ____________________________��
�������Ƕ���������������ۣ�������ȷ����_________________________���������գ���
a.ɱ��ˮ�еĸ��������������ʳ����Դ���ƻ�ˮ����̬ϵͳ
b.�Ե��ߡ����졢���������ݵȾ������������
c.�ƻ�������
d.�����������еĿ����ʷ�������ת��Ϊ�����Σ���ֲ���ṩ����
��2����ͼ�Ƕ�úȼ�ղ����ķ������г����������Ļ�������ʾ��ͼ����д���ڷ��������γɸ�����Ĺ���������������Ҫ��ѧ��Ӧ�Ļ�ѧ����ʽ_______��
��3�������Ժ��ڷ����к����������ӵIJ��������ǣ�д�������ƣ�_______�����Ի����ĸ���Ӱ����____________________________________________��
��4�����������������Ƿ���SO2�ļ�����_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
CO2��Ŀǰ�����к�����ߵ�һ���������塣��ˣ����ƺ�����CO2�ǽ������ЧӦ����Ч;����
��1�����й���CO2��˵����ȷ���ǣ�����ţ�_________��
�ټ��ٻ�ʯȼ�ϵ�ʹ�ã��������̫���ܡ����ܵ������Դ����Ч���ʹ�����CO2�ĺ���
��ֲ�����֣�����ֲ�����������Ч���ʹ�����CO2�ĺ���
�۶������������������̼���������ĺ������ǿ��������ձ�������
�ܿ�����CO2�ĺ������ᵼ��������γ�
��2�����д�ʩ���ܼ��ٶ�����̼�ŷŵ��ǣ�����ţ� _________��
������̫��������
�ڹ�ͣС�����ҵ
�۾��С�����һСʱ��Ϩ�ƻ
���ƹ�ʹ��úҺ������
��3�����з�Ӧ����������������ǣ�����ţ�_________��
���ô����Ʋ��� ����ú̿��ȼ��
��������ʯ���� ���ð���̼���
��4��Ŀǰ�����ڶ�����̼�Ƿ�Ϊ������Ⱦ���в�ͬ�Ĺ۵㡣��Ϊ��������̼���Ǵ�����Ⱦ��������ǣ�����ţ�_________��
�ٶ�����̼����Ҫ�Ļ���ԭ��
�ڶ�����̼��ֲ�������õıر�ԭ��
�۶�����̼����ɫ����ζ����������
�ܳ�������̼���⣬���顢һ����������Ҳ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ���ж��ֻ��ϼۣ����γɶ��ֻ����
��1����������1 mol��L��1 100 mL NaOH��Һǡ����ȫ����0.1 mol SO2���壬�˷�Ӧ�����ӷ���ʽΪ ������ҺpH_______7(�=����>������)��
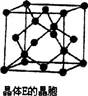
��2��ijͬѧ�ڳ������������ʵ������̽��Na2S2O3�Ļ�ѧ���ʡ�
ʵ��ٿ�˵��________(����ĸ)
| A����Na2S2O3��Һ��ˮ�����c(OH��)=10��8mol/L |
| B��H2S2O3��һ������ |
| C��Na2S2O3��һ��������� |
| D��Na2S2O3ˮ�ⷽ��ʽΪS2O32��+2H2O=H2S2O3+2OH�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com