
元素周期律的本质是------------------------------------------------------------------------( )
A、相对原子质量逐渐增大 B、核电荷数逐渐增大
C、核外电子排布呈周期性变化 D、元素的化合价呈周期性变化
科目:高中化学 来源: 题型:
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ⑤ | |||||
| 3 | ⑥ | ⑦ | ③ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ⅢA | ⅦA | ||||||||||||||||
| ① | ② | ③ | |||||||||||||||
| ④ | ⅢB | ⅦB | ⅡB | ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||
| ⑨ | Fe | ⑩ | |||||||||||||||
| E | |||||||||||||||||


查看答案和解析>>
科目:高中化学 来源: 题型:


图
(1)上表中的实线是元素周期表的部分边界,请在表中用实线补全元素周期表的边界。
(2)元素甲是第三周期、第ⅥA族元素,请在下边方框中按氦元素(图)的式样写出元素甲的原子序数、元素符号、元素名称、相对原子质量和最外电子层排布。

(3)元素乙的3p亚层中只有1个电子,则乙原子半径与甲原子半径比较:__________>__________。甲、乙的最高价氧化物水化物的酸性强弱为:_____________>___________(用化学式表示)。
(4)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的_____________,请写出元素在元素周期表中的位置与元素原子结构的关系:
_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界。
(2)元素甲是第三周期ⅥA族元素,请在下边方框中按氦元素的式样,写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
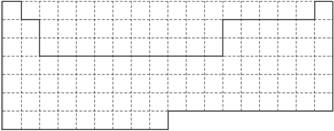

(3)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的____________,请写出元素在元素周期表中的位置与元素原子结构的关系:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com