
| A. | 燃烧反应都是放热反应 | |
| B. | 对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 | |
| C. | 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量 | |
| D. | 只有放热的氧化还原反应才可以设计为原电池 |
分析 A、燃烧就是发光、放热的剧烈的氧化还原反应;
B、△H=生成物的能量和-反应物的能量和;
C、反应热是反应物和生成物的能量差值;
D、反应物能量高于生成物时,化学能才可能转化为电能.
解答 解:A、燃烧就是发光、放热的剧烈的氧化还原反应,所以燃烧反应都是放热反应,故A正确;
B、△H=生成物的能量和-反应物的能量和,所以其逆反应的反应热是其相反数,故B正确;
C、氢气燃烧放热,说明氢气和氧气的能量和比水高,不变说明氢气比氧气能量高,故C错误;
D、反应物比生成物能量高时,才有能量转化为其他能量,故D正确;
故选:C.
点评 本题考查了燃烧的概念、反应热及其求算,题目难度不大,注意平时的知识积累.


科目:高中化学 来源: 题型:选择题
| 晶体类型 | 原子晶体 | 离子晶体 | 分子晶体 |
| A. | 氮化硅 | 磷酸 | 单质硫 |
| B. | 单晶硅 | 碳酸氢铵 | 水银 |
| C. | 金刚石 | 烧碱 | 冰 |
| D. | 铁 | 尿素 | 冰醋酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 所示.下列关于有机物 I的说法正确的是CD.
所示.下列关于有机物 I的说法正确的是CD.
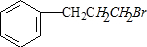 ;
; ;
; +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr.
+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg3N2+H2O═3Mg(OH)2+2NH3↑ | B. | NH3+CO2+H2O═NH4HCO3 | ||
| C. | 2NaOH+Cl2═NaCl+NaClO+H2O | D. | 2Na2O2+2CO2═2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 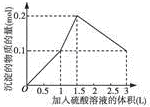 图A表示在1L含0.1mol NaAlO2和0.1mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.11mol•L-1H2SO4溶液,产生沉淀的物质的量与加入硫酸溶液体积的图象 | |
| B. | 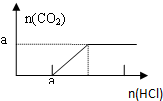 图B表示在分别含amol的Na2CO3和NaOH的混合溶液中逐滴滴加稀盐酸,产生气体 与加入盐酸体积的图象 | |
| C. | 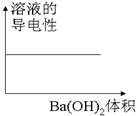 图C表示向100mL 0.1mol/L H2SO4溶液中,逐滴加入0.1mol/L Ba(OH)2溶液至过量, 溶液的导电性与加入 Ba(OH)2溶液体积的图象 | |
| D. | 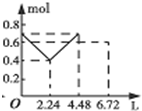 图D表示在往含0.2mol NaOH和0.1mol Ba(OH)2的溶液中持续稳定地通入CO2气体, 溶液中离子数目和通入CO2气体体积的图象(气体的溶解忽略不计) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
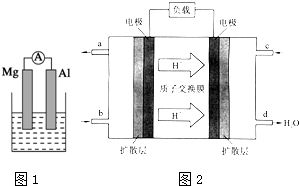 据图回答下列问题:
据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只能是离子化合物X2Y | |
| B. | 只能是共价化合物X2Y2 | |
| C. | 既可能是离子化合物也可能是共价化合物 | |
| D. | 形成的化合物无论是X2Y还是X2Y2 原子都达到了8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应结束后溶液的pH:甲>乙 | |
| B. | 反应开始时的速率:甲>乙 | |
| C. | 反应所需时间:甲<乙 | |
| D. | 反应开始时,酸的物质的量浓度:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com