
| 实验操作 | 实验现象 | 结论 | |
| A | 向硅酸钠溶液中滴加1滴酚酞,再逐滴加入稀盐酸至红色褪去 | 试管里出现凝胶 | 酸性:盐酸>硅酸 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| C | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 该溶液中一定含有SO42- |
| D | 向某无色溶液中先滴加氯水,再加少量CCl4,振荡,静置 | 溶液分层,下层为橙红色 | 溶液中含有Br- |
| A、A | B、B | C、C | D、D |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、称量时NaOH已经潮解 |
| B、定容时俯视容量瓶的标线 |
| C、向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过 |
| D、摇匀后发现液面低于标线,滴加蒸馏水至标线再摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
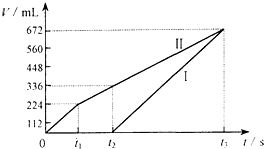 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于12.5% |
| B、大于12.5% |
| C、小于12.5% |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液、蒸发、萃取 |
| B、分液、萃取、加热 |
| C、分液、蒸馏、萃取 |
| D、蒸馏、加热、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42- |
| B、加入NaOH固体,产生的气体能使湿润红色石蕊试纸变蓝,则一定有NH4+ |
| C、先滴加氯水,再滴加KSCN溶液后显红色,则一定有Fe2+而没有Fe3+ |
| D、滴加硝酸银,生成白色沉淀,再滴加稀盐酸,沉淀不溶解,则含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 被提纯的物质 [括号内物质是杂质] | 除杂试剂 | 除杂方法 | |
| A | CO(g)[CO2(g)] | NaOH溶液、浓H2SO4 | 洗气 |
| B | NH4Cl(aq)[Fe3+(aq)] | NaOH溶液 | 过滤 |
| C | Cl2(g)[HCl(g)] | 饱和食盐水、浓H2SO4 | 洗气 |
| D | Na2CO3(s)[NaHCO3(s)] | - | 加热 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、SO32-、K+、Cl- |
| C、MnO4-、K+、SO42-、Na+ |
| D、K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com