
【题目】CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+![]() O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是________(填字母)。
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是________(填字母)。

a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C=O键断裂,则反应达最大限度
(2)某温度下,将5 mol CH3OH和2 mol O2充入2 L的密闭容器中,经过4 min反应达到平衡,测得c(O2)=0.2 mol·L-1,4 min内平均反应速率v(H2)=________,则CH3OH的转化率为_______________。
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是________(填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4 g CH3OH转移1.2 mol电子
(4)写出CH3OH燃料电池在酸性条件下负极的反应式______________
【答案】cd 0.8mol/(L·min) 64% ②③ CH3OH+H2O-6e-═CO2↑+6H+
【解析】
(1)由图可知,反应物总能量小于生成物总能量,反应为放热反应,结合化学反应的本质和平衡的特征分析判断;
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2molL-1,则氧气的浓度变化量为:![]() -0.2mol/L=0.8mol/L,再根据三段式分析计算;
-0.2mol/L=0.8mol/L,再根据三段式分析计算;
(3)CH3OH燃料电池中通入燃料甲醇的电极为负极,通入空气的电极为正极,结合电解质溶液为氢氧化钾分析判断;
(4)负极发生氧化反应,甲醇在负极失去电子,酸性条件下生成CO2,据此书写电极反应式。
(1)a.由图可知,反应物总能量小于生成物总能量,为放热反应,故a错误;b.速率之比等于其化学计量数之比,H2的生成速率与CH3OH的消耗速率之比为2∶1,故b错误;c.化学变化的本质是旧的化学键断裂,原子总组合生成新物质,形成新的化学键,化学变化不仅有新物质生成,同时也一定有能量变化,故c正确;d.1mol H-O键断裂的同时2mol C=O键断裂,分别表示正、逆反应速率,等于化学计量数之比,正逆反应速率相等,反应到达平衡,故d正确;故答案为:cd;
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2molL-1,则氧气的浓度变化量为:![]() -0.2mol/L=0.8mol/L,
-0.2mol/L=0.8mol/L,
CH3OH(g)+![]() O2(g)CO2(g)+2H2(g)
O2(g)CO2(g)+2H2(g)
起始浓度(mol/L):2.5 1 0 0
变化浓度(mol/L):1.6 0.8 1.6 3.2
平衡浓度(mol/L):0.9 0.2 1.6 3.2
故v(H2)=![]() =0.8mol/(L·min),CH3OH的转化率=
=0.8mol/(L·min),CH3OH的转化率=![]() ×100%=64%,故答案为:0.8mol/(L·min);64%;
×100%=64%,故答案为:0.8mol/(L·min);64%;
(3)①CH3OH燃料电池中通入燃料甲醇的电极为负极,通入空气的电极为正极,故①错误;②电池放电时负极发生氧化反应,甲醇在负极失去电子,碱性条件下生成碳酸根离子,负极电极反应式为:CH3OH+8OH--6e-═CO32-+6H2O,电解质溶液的碱性逐渐减弱,故②正确;③6.4gCH3OH的物质的量为![]() =0.2mol,碱性条件下,CH3OH为氧化为CO32-,转移电子为0.2mol×6=1.2mol,故③正确;故答案为:②③;
=0.2mol,碱性条件下,CH3OH为氧化为CO32-,转移电子为0.2mol×6=1.2mol,故③正确;故答案为:②③;
(4)负极发生氧化反应,甲醇在负极失去电子,酸性条件下生成CO2,根据电荷守恒可知,有氢离子生成,负极电极反应式为:CH3OH+H2O-6e-═CO2↑+6H+,故答案为:CH3OH+H2O-6e-═CO2↑+6H+。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)被称为21世纪的新型燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
(1)该工艺的总反应为3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g) ΔH=_________,化学平衡常数K=______________(用含K1、K2、K3的代数式表示)。
CH3OCH3(g)+CO2(g) ΔH=_________,化学平衡常数K=______________(用含K1、K2、K3的代数式表示)。
化学反应方程式 | 化学平衡常数 | |
①CO(g)+2H2(g) | ΔH1=-99 kJmol-1 | K1 |
②2CH3OH(g) | ΔH2=-24 kJmol-1 | K2 |
③CO(g)+H2O(g) | ΔH3=-41 kJmol-1 | K3 |
(2)某温度下,将8.0molH2和4.0molCO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g) ![]() CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则用H2表示的反应速率为_________,CO的转化率为________。
CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则用H2表示的反应速率为_________,CO的转化率为________。
(3)下列措施中,能提高CH3OCH3产率的有________。
A.分离出二甲醚 B.降低温度 C.改用高效催化剂D.增大压强
(4)该工艺中反应③的发生提高了CH3OCH3的产率,原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素原子序数依次喊小,原子半径的大小关系为:r(Y)>r(X)>r(Z), 三种元素的原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法不正确的是( )

A. X元素位于ⅥA族 B. A难溶于B中
C. A和C不可能发生氧化还原反应 D. B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将3 mol A气体和1 mol B气体混合于固定容积为2 L的密闭容器中,发生反应:3A(g)+B(g) ![]() C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
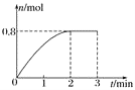
A. 若混合气体的密度不再改变时,该反应不一定达到平衡状态
B. 2 min后,加压会使正反应速率加快,逆反应速率变慢
C. 反应过程中A和B的转化率之比为3∶1
D. 开始到平衡,用A表示的化学反应速率为0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)p电子的原子轨道呈______形;
(2)共价键的类型有两种分别是σ键和π键,σ键的对称方式为______;
(3)某元素位于元素周期表中第四周期,第VA族,元素符号是______,最高价氧化物对应的水化物的化学式______;
(4)用“>”或“<”填空:①能量:4p______5s②离子半径:F-______Na+;
(5)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。
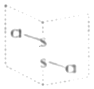
①S2Cl2的结构式为______,其化学键类型有______(填“极性键”“非极性键”或“极性键和非极性键”)。
②电负性:S______Cl(填“>”或“<”),每个S原子有______对弧电子对。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定为3 L的某密闭容器中加入1 mol A、2 mol B,一定温度下发生如下反应:A(s)+2B(g)![]() C(g)+D(g),经反应5 min后,测得C的浓度为0.3 mol·L-1。则下列说法中正确的是
C(g)+D(g),经反应5 min后,测得C的浓度为0.3 mol·L-1。则下列说法中正确的是
A. 5 min内D的平均反应速率为0.02 mol·L-1·min-1
B. 5 min内A的平均反应速率为0.06 mol·L-1·min-1
C. 经5 min后,向容器内再加入C,正反应速率变小
D. 平衡状态时,生成1 mol D时同时生成1 mol A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氮肥厂氨氮废水中的氮元素多以NH4+和NH3![]() H2O的形式存在,该废水的处理流程如下:
H2O的形式存在,该废水的处理流程如下:
![]()
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:____________。
②用化学平衡原理解释通空气的目的:__________。
(2) 过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
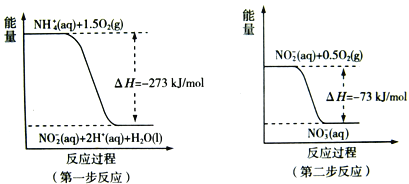
①第一步反应是_________反应(选题“放热”或“吸热”),判断依据是__________。
②1mol NH4+(aq)全部氧化成![]() 的热化学方程式是______________。
的热化学方程式是______________。
(3) 过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗![]() 转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是__________。
转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素。如图是实验室从海藻里提取碘的流程的一部分。下列判断正确的是

A. 步骤④的操作是过滤
B. 可用淀粉溶液检验步骤②的反应是否进行完全
C. 步骤①、③的操作分别是过滤、萃取
D. 步骤③中加入的有机溶剂可能是酒精或四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以链烧烃 (C4H6) 和丙烯醛( CH2= CHCHO) 为原料合成某药物中间体环戊基甲酸(部分反应条件、产物已省略),其流程如下:
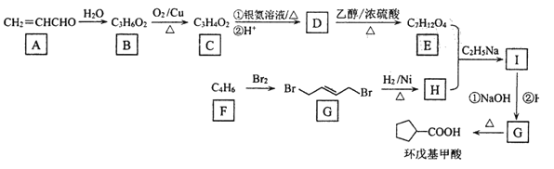
已知:i.![]() +2RBr
+2RBr 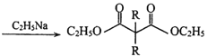 +2HBr
+2HBr
ii. ![]() +2CO2
+2CO2
请回答下列问题:
(1) B中的官能团名称为________,D→E的反应类型是 ____________ .
(2)写出C与银氨溶液反应的化学方程式①:_____________ 。
(3)一定条件下,H可制取F, 则所需试剂和反应条件是____________________ 。
(4) I的结构简式为______________。
(5)环戊基甲酸与苯酚反应生成一种酯X,写出一种同时符合以下条件的 X 的同分异构体的结构简式:________(不考虑立体异构)。
①核磁共振氢谱有四组峰,峰面积比为9:2:2:l
②能与FeCl3发生显色反应
③与浓溴水反应时,l molX可消耗4mol Br2
(6)参照上述合成路线,设计以乙醇和化合物E为原料制备2.2-二乙基丙二酸(结构简式: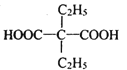 )的合成路线(无机试剂任选):___________________。
)的合成路线(无机试剂任选):___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com