
【题目】CuSO4溶液与Na2CO3溶液混合时产生蓝绿色沉淀,某实验小组进行实验,探究蓝绿色沉淀的组成。
【查阅资料】
i.氢氧化铜是一种蓝色絮状沉淀,难溶于水,溶于酸、氨水等,受热会分解。
ii.碳酸铜是蓝绿色粉末状固体,受热易分解,遇水转化为氢氧化铜和碱式碳酸铜的混合物。
iii.碱式碳酸铜呈孔雀绿颜色,又叫孔雀石,难溶于水,溶于酸、氨水等,在空气中加热会分解。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为CuCO3
假设3:沉淀为碱式碳酸铜[化学式可表示为xCuCO3yCu(OH)2]
(1)假设1中产生沉淀Cu(OH)2的离子方程式是_______。
(2)甲同学认为假设2不成立,理由是_______。
【定性实验】
(3)实验小组同学将沉淀从溶液中分离并净化,取少量净化后的固体于试管中,滴加稀硫酸,观察到_______,证明假设3成立。
【定量实验】
为了确定碱式碳酸铜化学式中x与y的关系,实验小组称取净化后的蓝绿色固体m1 g,使用下列装置(夹持仪器未画出)进行实验。
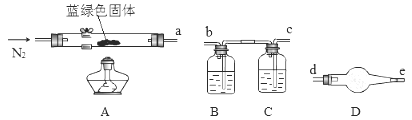
(4)B、C、D中的试剂依次为_______(填标号)。
a.澄清石灰水 b.碱石灰 c.氯化钙溶液 d.浓硫酸
(5)各装置接口的连接顺序:a→_______(填字母序号)。
(6)装置D的作用是_______。
(7)加热到固体完全分解,硬质玻璃管中得到黑色固体,其余产物被相应装置完全吸收。实验结束后,测得装置B的质量增加m2 g,则xCuCO3yCu(OH)2中![]() =_______(列式表示)。若无D装置,则
=_______(列式表示)。若无D装置,则![]() 的值_______(填“偏大”或“偏小”或“无影响”)。
的值_______(填“偏大”或“偏小”或“无影响”)。
【答案】 Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑ 碳酸铜遇水会发生双水解,转化为氢氧化铜和碱式碳酸铜的混合物 蓝绿色沉淀溶解,产生气泡,溶液呈蓝色 adb c b→d或cbd或cbde 防止空气中的二氧化碳进入装置B,影响测定结果  偏大
偏大
【解析】本题主要考查对于探究CuSO4溶液与Na2CO3溶液混合时产生蓝绿色沉淀成分实验的评价。
(1)假设1中产生沉淀Cu(OH)2的离子方程式是Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑。
(2)甲同学认为假设2不成立,理由是碳酸铜遇水转化为氢氧化铜和碱式碳酸铜的混合物。
(3)实验小组同学将沉淀从溶液中分离并净化,取少量净化后的固体于试管中,滴加稀硫酸,观察到蓝绿色沉淀溶解,产生气泡,溶液呈蓝色,证明假设3成立。
(4)C用来吸水水蒸气,B用来吸收二氧化碳,D用来吸收空气中的二氧化碳,所以B、C、D中的试剂依次为adb。
(5)各装置接口的连接顺序:a→cb→de。
(6)装置D的作用是防止空气中的二氧化碳进入装置B而影响测定结果。
(7)装置B吸收的二氧化碳的物质的量为m2 /44mol,CuCO3的质量为31/11m2 g,Cu(OH)2的质量为(m1-124/44m2) g,物质的量为(m1-124/44m2)/98mol,则xCuCO3yCu(OH)2中![]() =
= 。若无D装置,x增大,则
。若无D装置,x增大,则![]() 的值偏大。
的值偏大。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质中,可按溶解、过滤、蒸发结晶的操作顺序分离的是( )
A.CaO和KCl
B.CuO和NaCl
C.BaSO4和CaCO3
D.NaCl和AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一束强光照射Fe(OH)3是胶体,我们在于光线垂直的方向可以看到一条光的通路,胶体的这种特性,叫做______,在该分散系中,分散质微粒的直径大约在______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态水,同时放出22.68kJ热量,下列表示该反应的热化学方程式的是( )
A. CH3OH(l)+![]() O2===CO2(g)+2H2O(l) △H =-725.8kJ/mol
O2===CO2(g)+2H2O(l) △H =-725.8kJ/mol
B. 2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) △H =+145.6kJ/mol
C. 2CH2OH(l)+3O2(g)====2CO2(g)+4H2O(l) △H =-22.68kJ/mol
D. CH3OH(l) +![]() O2(g)===CO2(g)+2H2O(g) △H =-725.8kJ/mol
O2(g)===CO2(g)+2H2O(g) △H =-725.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液,有关粒子的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。下列说法正确的是

A. M点溶液中:2c(HA-)+c(A2-)=0.2 mol/L
B. N点溶液呈酸性,则c(Na+) < 3c(HA-)
C. 若N点溶液pH =4.2,则Ka2(H2A)的数量级为104
D. V(NaOH)=20mL时,溶液中:c(H+) < c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,对社会发展与进步作出了巨大贡献。
(1)450℃时,在一个体积为2L的恒容密闭容器中充入0.4 mol N2和0.6 mol H2(10min时改变某一条件),测得反应过程中N2、H2和NH3的物质的量随时间变化如下表:
时间 物质的量 | 5 min | 10 min | 15 min | 20 min | 25 min |
n(N2)/mol | 0.36 | 0.35 | 0.275 | 0.25 | 0.25 |
n(H2)/mol | 0.48 | 0.45 | 0.225 | 0.15 | 0.15 |
n(NH3)/mol | 0.08 | 0.1 | 0.25 | 0.30 | 0.30 |
①5~10 min内,生成NH3的平均反应速率是_______ mol/(L·min)。
②下列能作为判断该反应达到化学平衡状态的依据是_______(填字母序号)。
A.v(N2)正=3v(H2)逆 B.容器内压强保持不变
C.容器内混合气体的密度保持不变 D.容器内混合气体的平均相对分子量不变
③第10 min时改变的条件是使用了高效催化剂,理由是_______。
(2)合成氨的反应原理为:N2(g)+3H2(g)![]() 2NH3(g) ΔH。
2NH3(g) ΔH。
相关化学键键能数据如下:
化学键 | H—H | N≡N | N—H |
E /(kJ/mol) | 436 | 946 | 391 |
由此计算ΔH=_______kJ/mol,低温下,合成氨反应_______(填“能”或“不能”)自发进行。已知合成氨反应N2(g)+3H2(g)![]() 2NH3(g)的活化能Ea1=499kJ/mol,由此计算氨分解反应2NH3(g)
2NH3(g)的活化能Ea1=499kJ/mol,由此计算氨分解反应2NH3(g)![]() N2(g)+3H2(g)的活化能Ea2=_______kJ/mol。
N2(g)+3H2(g)的活化能Ea2=_______kJ/mol。
(3)已知:氨在某催化剂催化氧化过程中主要有以下两个竞争反应:
反应Ⅰ:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H =﹣906kJ/mol
4NO(g)+6H2O(g) △H =﹣906kJ/mol
反应II:4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H =﹣1267kJ/mol
2N2(g)+6H2O(g) △H =﹣1267kJ/mol
①该条件下,N2(g)+O2(g)![]() 2NO(g) △H = _______kJ/mol
2NO(g) △H = _______kJ/mol
②为分析催化剂对反应的选择性,在1 L密闭容器中充入1 mol NH3和2 mol O2,测得有关物质的物质的量随温度变化如图所示。

该催化剂在较低温度时主要选择反应_______(填“反应Ⅰ”或“反应II”)。520℃时,反应Ⅰ的平衡常数K=_______(只列算式不计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2A为二元弱酸,20℃时,配制一组c(H2A)+c(HA-)+c(A2-)=0.100mol/L的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法错误的是

A. Ka2(H2A)的数量级为10-5
B. NaHA溶液中:c(H+)>c(OH-)
C. M点由水电离出的c(H+)>N点由水电离出的c(H+)
D. pH=7的溶液中:c(Na+)>2c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生活生产中常见物质的主要成分的化学式与名称相对应的是
A. 光导纤维——SiO2 B. 漂粉精——Ca(C1O3)2
C. 碱石灰——Na2CO3 D. 绿矾一Fe2(SO4)3·7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com