
【题目】已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( ) 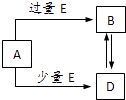
A.若A是铁,则E可能为稀硝酸
B.若A是CuO,E是碳,则B为CO
C.若A是AlCl3溶液,E可能是氨水
D.若A是NaOH溶液,E是CO2 , 则B为NaHCO3
【答案】C
【解析】A、A为Fe和硝酸反应可以生成硝酸铁和硝酸亚铁,硝酸亚铁可以被氧化为硝酸铁,能实现上述转化,故A不符合;B、A为CuO,碳还原氧化铜生成铜和二氧化碳,二氧化碳被过量碳还原为一氧化碳,符合上述反应转化,故B不符合;
C、若A是AlCl3溶液,和氨水反应生成氢氧化铝沉淀,氢氧化铝不溶于氨水,不能实现转换,故C符合;
D、若A是NaOH溶液,二氧化碳和氢氧化钠溶于反应可以生成碳酸钠和碳酸氢钠,碳酸钠和碳酸氢钠可以相互转化,符合上述转化,故D不符合;
故选C.
A、A为Fe和硝酸反应可以生成硝酸铁和硝酸亚铁,硝酸亚铁可以被氧化为硝酸铁;
B、A为CuO,碳还原氧化铜生成铜和二氧化碳,二氧化碳被过量碳还原为一氧化碳;
C、若A是AlCl3溶液,和氨水反应生成氢氧化铝沉淀,氢氧化铝不溶于氨水,不能实现转换;
D、若A是NaOH溶液,二氧化碳和氢氧化钠溶于反应可以生成碳酸钠和碳酸氢钠,碳酸钠和碳酸氢钠可以相互转化;


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】把6molA和5molB两气体通入容积为4L的密闭容器中,一定条件下反应:3A(g)+B(g) ![]() 2C(g)+xD(g);△H<0,5min达平衡,此时生成2molC,测得D的平均反应速率为0.1mol(Lmin)﹣1 . 下列说法中正确的是( )
2C(g)+xD(g);△H<0,5min达平衡,此时生成2molC,测得D的平均反应速率为0.1mol(Lmin)﹣1 . 下列说法中正确的是( )
A.A的平均反应速率为0.15mol(Lmin)﹣1
B.恒温下达到平衡的标志是C和D的生成速率相等
C.降低温度,逆反应速率变小,正反应速率增大,平衡正向移动
D.B的转化率为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A. 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
B. 取a克混合物与足量稀硫酸充分反应,逸出气体未经干燥用碱石灰吸收,增重b克
C. 取a克混合物充分加热至恒重,减重b克
D. 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.14C与12C互为同素异形体B.甘氨酸和硝基乙烷互为同分异构体
C.乙二醇和甘油互为同系物D.14N2与15N2是两种不同的核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g)△H<0,下列各项对示意图的解释与图象相符的是( ) 
A.①压强对反应的影响(p2>p1)
B.②温度对反应的影响
C.③平衡体系增加N2对反应的影响
D.④催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾(KMnO4)是一种常用的氧化剂.不同条件下高锰酸钾可发生如下反应:
①MnO4﹣+5e﹣+8H+═Mn2++4H2O
②MnO4﹣+3e﹣+2H2O═MnO2+4OH﹣
③MnO4﹣+e═MnO42﹣(溶液绿色)
(1)从上述三个半反应中可以看出MnO4﹣的还原产物与溶液的有关.
(2)用草酸(H2C2O4)的稀溶液可以洗涤粘在皮肤上的高锰酸钾,其中的变化:H2C2O4→CO2↑.写出该反应的离子方程式: .
(3)将PbO2粉末投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的是(填字母).
a.氧化性强弱:PbO2>KMnO4
b.还原性强弱:PbO2>KMnO4
c.该反应可以用盐酸酸化
d.PbO2发生还原反应:PbO2+SO42﹣+4H++2e﹣═PbSO4+2H2O
(4)用KMnO4可以测定H2O2溶液的有效含量:取15.00mL某浓度H2O2溶液,逐滴加入0.03mo1L﹣1 KMnO4溶液(已酸化),产生无色气体,至终点时共消耗20.00mL KMnO4溶液.
①写出反应的离子方程式;
②溶液中c(H2O2)=molL﹣1;
③反应中转移电子数目mo1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应:2A(g)B(g)+C(g)的平衡常数为1,在容积为2L的密闭容器中加入A(g),20s时测得各组分的物质的量如下表:下列说法正确的是( )
物质 | A(g) | B(g) | C(g) |
物质的量/mol | 1.2 | 0.6 | 0.6 |
A.反应前20 s内的平均反应速率为v(A)=0.6 molL﹣1s﹣1
B.20 s时,正反应速率大于逆反应速率
C.达到平衡时,A(g)的转化率为100%
D.若升高温度平衡常数变为2,则反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com