
含有下列各组离子的溶液中通入(或加入)过量的某种物质后仍能大量共存的是
A.H+、Ba2+、Fe3+、NO3-,通入SO2气体
B.Ca2+、Cl-、K+、H+,通入CO2气体
C.AlO2-、Na+、Br-、SO42-,通入CO2气体
D.HCO3-、Na+、I-、HS-,加入AlCl3溶液
科目:高中化学 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:选择题
对于反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,在测量化学反应速率时,以下相关性质不可以利用的为( )
A.气体的体积和体系的压强
B.溶液颜色的深浅
C.H+浓度的变化
D.固体物质的体积
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:选择题
分析下列反应在任何温度下均能自发进行的是( )
A.2N2(g)+O2(g)===2N2O(g)ΔH=+163 kJ·mol-1
B.Ag(s)+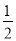 Cl2(g)===AgCl(s)ΔH=-127 kJ·mol-1
Cl2(g)===AgCl(s)ΔH=-127 kJ·mol-1
C.HgO(s)===Hg(l)+ O2(g) ΔH=+91 kJ·mol-1
O2(g) ΔH=+91 kJ·mol-1
D.H2O2(l)===  O2(g)+H2O(l) ΔH=-98 kJ·mol-1
O2(g)+H2O(l) ΔH=-98 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:填空题
Ⅰ.饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质。A、B、C、D、E五种常见化合物都是由下表中的离子形成:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为____________。
(2)写出实验②发生反应的离子方程式: 。
(3)C常用作净水剂,用离子方程式表示其净水原理: 。
Ⅱ.某强酸性溶液X可能含有A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-中的若干种,取该溶液进行连续实验,实验过程及产物如下:

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子有_____________肯定不存在的离子是_________________
(2)请设计简单的实验检验不能确定是否含有的离子(若不止一种,可任选一种)的存在:____________________。
(3)写出反应①的离子方程式:________________。
(4)假设测定A、F、I均为0.1mol,100mL X溶液中n(H+)=0.4mol,当沉淀C的物质的量大于0.7mol时,溶液X中还一定含有____________.
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:选择题
下列各项反应对应的图像正确的是
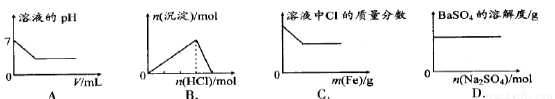
A.25℃时,向亚硫酸溶液中通入氯气
B.向 Na[Al(OH)4]溶液中通入 HCl气体
C.向少量氯化铁溶液中加入铁粉
D.向 BaSO4饱和溶液中加入硫酸钠
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:选择题
下列关于胶体的叙述正确的是
A.过滤实验可以据此把胶体、溶液分开
B.胶体和溶液的本质区别是胶体能发生丁达尔现象
C.用渗析的方法净化胶体时,使用半透膜只能让小分子和离子通过
D.胶体带电,故在电场作用下会产生电泳现象
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:填空题
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为________________;己知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是____________________。
(2)硒、硅均能与氢元素形成气态氢化物,若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se___________Si(填“>”、“<”)。与Si同周期部分元素的电离能如下图所示,其中a、b和c分别代表____________。
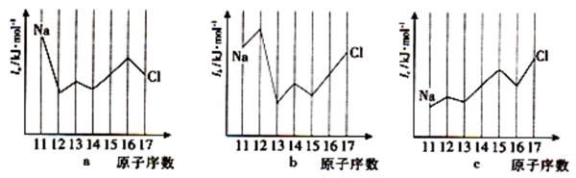
A.a为Il、b为I2、c为I3B.a为I2、b为I3、c为I1
C.a为I3、b为I2、c为I1D.a为Il、b为I3、c为I2
(3) SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为____________;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_____________。
(4)镓与某有机物形成的配合物过程如下图(左),在图上画出产物中的配位键。
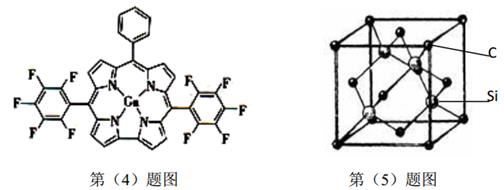
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如上图(右)所示,则Si原子的配位数为___________,每个C原子周围最近的C原子数目为___________个;若晶胞的边长为a pm,则金刚砂的密度表达式为___________g/cm3。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列说法错误的是( )
A.18g冰的晶体中含有氢键的数目为2NA
B.11.2 L丙烷(标准状况)中含有σ键的数目为5NA
C.2.0 L 0.5 mol/L NaAlO2溶液中含有氧原子的数目为2NA
D.1molCl2与足量NaOH溶液反应,转移电子的数目为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第二次月考化学卷(解析版) 题型:填空题
高纯度氧化铝有广泛的用途,某研究小组用以下流程制取高纯度氧化铝:

根据上述流程图填空:
(1)“除杂”操作是先加入过氧化氢充分反应后,再用氨水调节溶液的pH,使硫酸铵溶液中的少量Fe2+氧化为Fe3+并进一步转化为Fe(OH)3从而除去Fe2+,则Fe2+酸性条件下氧化为Fe3+的离子方程式为:
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(3)“分离”操作的名称是 (填字母代号)。
A.蒸馏 B.分液 C.过滤
(4)铵明矾晶体的化学式为NH4Al(SO4)2•12H2O,铵明矾属于 (填“纯净物”或“混合物”)在0.1mol/L铵明矾的水溶液中,浓度最大的离子是 。
(5)热分解中发生如下反应6NH4Al(SO4)2 = 3Al2O3 + 2NH3 ↑+ 2N2 ↑+ 6SO2 ↑+ 6SO3 ↑+ 9H2O,当生成1mol Al2O3时转移电子物质的量为 mol
(6)往含0.1mol铵明矾稀溶液中逐滴加入含0.3mol Ba(OH)2的稀溶液,反应的总离子方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com