
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
A
【解析】
试题分析:由题意可知,阴极发生反应的是Cu2++2e-===Cu,铜离子放电完全后是氢离子放电,发生2H++2e-==H2↑,阳极一直是氢氧根离子放电生成氧气,2H2O -4e- =O2↑+4H+;当两极都生成2.24L气体,物质的量是0.1mol时,则生成0.1mol氧气转移电子的物质的量是0.4mol,生成0.1mol氢气时得到电子的物质的量是0.2mol,根据得失电子守恒,铜离子应得0.2mol电子,则原溶液中含有铜离子的物质的量是0.1mol,其浓度是0.1mol/0.5L=0.2mol/L,根据溶液为电中性,所以c(K+)+ 2c(Cu2+)= c(NO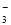 ),所以 c(K+)=0.2 mol·L-1,A正确;上述过程中应转移0.4mol电子,B错误;电解得到的Cu的物质的量是0.1mol,C错误;根据生成氧气的物质的量可知同时生成0.4mol 氢离子,而生成0.1mol氢气时消耗0.2mol氢离子,所以整个过程中产生0.2mol氢离子,电解后溶液中c(H+)=0.2 mol/0.5L=0.4 mol·L-1,错误,答案选A。
),所以 c(K+)=0.2 mol·L-1,A正确;上述过程中应转移0.4mol电子,B错误;电解得到的Cu的物质的量是0.1mol,C错误;根据生成氧气的物质的量可知同时生成0.4mol 氢离子,而生成0.1mol氢气时消耗0.2mol氢离子,所以整个过程中产生0.2mol氢离子,电解后溶液中c(H+)=0.2 mol/0.5L=0.4 mol·L-1,错误,答案选A。
考点:考查电解反应的计算,离子放电顺序的应用


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年浙江省绍兴市高一上学期期中化学试卷(解析版) 题型:选择题
向四支试管中分别加入少量不同的无色溶液进行如下操作,现象和结论正确的是
| 操作 | 现象 | 结论 |
A. | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B. | 先滴加稀盐酸再滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl- |
C. | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
D. | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市十校联合体高一上学期期中联考化学试卷(解析版) 题型:选择题
下列分离方法中不正确的是
A.利用萃取方法用四氯化碳提取溴水中的溴单质
B.利用蒸馏的方法可以分离沸点相差较大的液体混合物
C.利用结晶的方法除去KNO3中的氯化钠
D.利用分液的方法分离酒精和水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州市高二10月月考化学试卷(解析版) 题型:实验题
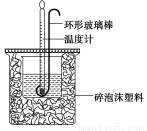
(6分)实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
试完成下列问题:
(1)实验时用环形玻璃棒搅拌溶液的方法是_______________________________________。
不能用铜丝搅拌棒代替环形玻璃棒的理由是________________________。
(2)经数据处理,t2—t1=3.4 ℃。则该实验测得的中和热ΔH=________[盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1________ΔH(填“<”、“>”或“=”),理由是__________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州市高二10月月考化学试卷(解析版) 题型:选择题
用惰性电极实现电解,下列说法正确的是
A.电解氢氧化钠稀溶液,溶液浓度增大pH变小
B.电解氯化钠溶液,溶液浓度减小pH不变
C.电解硝酸银溶液,要消耗OH--溶液pH变小
D.电解稀硫酸,实质是电解水,溶液pH不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州市高二10月月考化学试卷(解析版) 题型:选择题
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是。
A.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州市高二10月月考化学试卷(解析版) 题型:选择题
已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是 ( )。

A.每生成2分子AB吸收b kJ热量
B.该反应热ΔH=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州市高一10月月考化学试卷(解析版) 题型:选择题
已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高。则下列溶液沸点最高的是
A.0.01 mol·L-1的蔗糖溶液 B.0.01 mol·L-1的CaCl2溶液
C.0.02 mol·L-1的NaCl溶液 D.0.02 mol·L-1的CH3COOH溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省东阳外国语学校高二上学期期中化学试卷(解析版) 题型:实验题
(14分)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量,某实验小组做了如下实验:
Ⅰ.称量4.910g三草酸合铁酸钾晶体,配制成250mL溶液。
Ⅱ.取所配溶液25.00mL于锥形瓶中,加稀硫酸酸化,滴加KMnO4溶液至草酸根(C2O42?)恰好全部氧化成二氧化碳,同时MnO4?被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液的黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
Ⅲ.用0.01000mol/L KMnO4溶液滴定步骤Ⅱ所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4?被还原成Mn2+ 。
Ⅳ.重复步骤Ⅱ、步骤Ⅲ操作,滴定消耗0.01000mol/L KMnO4溶液19.98mL
请回答下列问题:
(1)滴定过程中需添加的指示剂是(若不需要请说明理由)
(2)加入锌粉的目的是 。
(3)写出步骤Ⅲ中发生反应的离子方程式 。
(4)实验测得该晶体中铁的质量分数为 ;X= 。
(5)在步骤Ⅱ中,若加入的KMnO4的溶液的量不够,则测得的铁含量 ;(选填“偏低”“偏高”“不变”,下同)若加入的锌粉的量不够,则测的铁的含量 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com