
【题目】某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42ˉ、SiO32ˉ、NO3ˉ中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。

请回答下列问题:
(1)由强酸性条件即可判断溶液X中一定不存在的离子有:
(2)溶液X中,关于NO3ˉ的判断一定正确的是;
a.一定有
B.一定没有
C.可能有
(3)产生气体A的离子方程式为;
(4)转化⑥发生反应的现象为;
(5)转化④中产生H的离子方程式为;
(6)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为;
(7)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是。
①NaOH溶液,②KSCN溶液,③石蕊试剂,④pH试纸,
⑤KMnO4溶液,⑥氯水和KSCN的混合溶液
【答案】(1)CO32ˉ、SiO32ˉ(2)b
(3)3Fe2++NO3ˉ+4H+=2Fe3++NO+2H2O
(4)红褐色沉淀溶解,溶液呈黄色
(5)Al3++4OHˉ=AlO2ˉ+2H2O
(6)4:1
(7)②
【解析】试题分析:某强酸性溶液X,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液呈存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,A是NO;溶液B中加入氢氧化钠溶液时,产生气体F,则溶液中含有NH4+,F是NH3,产生沉淀,则溶液中存在Fe3+,沉淀G是Fe(OH)3,氢氧化铁和盐酸反应生成FeCl3,则J是FeCl3,溶液H中通入过量二氧化碳生成沉淀,则溶液中存在Al3+,沉淀K是Al(OH)3,溶液L是NaHCO3;A是NO,则D是NO2,二氧化氮化和水反应生成硝酸和NO,则E是HNO3,硝酸和氨气反应生成硝酸铵,则I是NH4NO3。
(1)由强酸性条件即可判断溶液X中一定不存在弱酸根离子,所以不存在的离子有CO32-、SiO32-;
(2)强酸性溶液中硝酸根离子具有强氧化性,如果存在硝酸根离子,则不存在亚铁离子,加入硝酸钡溶液时不能产生气体,所以溶液X中一定没有NO3-,答案选b;
(3)亚铁离子和硝酸反应生成铁离子、一氧化氮和水,离子反应方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)氢氧化铁和稀盐酸反应生成氯化铁和水,氢氧化铁为红褐色沉淀,氯化铁溶液呈黄色,所以看到的现象是:红褐色沉淀逐渐溶解,溶液变为黄色;
(5)铝离子和过量氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为:Al3++4OH-=AlO2-+2H2O;
(6)若转化③中,NO2、H2O、O2三种物质恰好发生化合反应生成HNO3,该反应方程式为:4NO2+2H2O+O2=4HNO3,则反应中D与O2的物质的量之比为4:1;
(7)溶液中铁离子是否存在不能确定,铁离子和硫氰化钾溶液反应生成血红色溶液,所以可以用硫氰化钾溶液检验,答案选②。


科目:高中化学 来源: 题型:
【题目】两只敞口烧杯中分别发生如下反应:一只烧杯中反应为:A+B=C+D,反应温度为T1,另一只烧杯中反应为:M+N=P+Q,反应温度为T2,T1>T2,则两只烧杯中反应速率快慢为
A.前者快 B.后者快 C.一样快 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的锌与过量的稀H2SO4反应制取氢气,一定温度下为减慢反应速率而又不影响生成氢气的量,可向其中加入
A. KCl固体 B. 铁粉
C. K2SO4溶液 D. KNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应中,反应类型与其他反应不同的是( )
A.甲烷与氯气混合后光照
B.以苯为原料制备溴苯
C.由1,2-二溴乙烷制备1,2-乙二醇
D.一定条件下甲苯转化为苯甲酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低温迫使植物细胞产生大量对细胞有害的过氧化物,如脂质过氧化物(MDA)。超氧化物歧化酶(SOD)能够消除过氧化物,从而增强植物的抗冷性。研究人员进行了“水杨酸对水稻幼苗抗冷性的影响”实验,实验步骤及结果如表所示。
组别 | 处理 | 培养温度 /℃ |
|
1 | 蒸馏水浇灌 | 25 | 7.3 |
2 | ① | ② | 9.4 |
3 | 0.5 mmol/L水杨酸浇灌 | 5 | 10.3 |
4 | 1.0 mmol/L水杨酸浇灌 | 5 | 11.6 |
5 | 1.5 mmol/L水杨酸浇灌 | 5 | 13.6 |
6 | 2.0 mmol/L水杨酸浇灌 | 5 | 8.5 |
7 | 2.5 mmol/L水杨酸浇灌 | 5 | 7.9 |
8 | 3.0 mmol/L水杨酸浇灌 | 5 | 6.5 |
(1)表中①是 ,②是 ,其的作用为 ,实验设计时每组取50株水稻幼苗,而不是1株,目的是 。
(2)本实验自变量为 , ,需要控制的无关变量有 , (至少写两个)。
(3)组别1和2对照可得的结论是 。对比组别2~8可得的结论是 。
(4)在5 ℃的环境下,物质的量浓度为2.0 mmol/L的水杨酸对水稻幼苗抗冷性的影响是 (填“增强”或“减弱”)。
(5)请根据5 ℃条件下的实验结果完成水杨酸浓度—SOD活性关系的坐标曲线图。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图曲线Ⅰ、Ⅱ分别表示物质A在无催化条件和有酶催化条件下生成物质P所需的能量变化过程.下列相关叙述正确的是
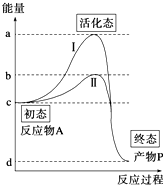
A.ad段表示在无催化剂条件下,物质A生成物质P需要的活化能
B.若将酶催化改为无机催化剂催化该反应,则b在纵轴上将向下移动
C.若仅增加反应物A的量,则图中曲线的原有形状均发生改变
D.若曲线Ⅱ为最适酶促条件下的曲线,改变酶促条件后,则b在纵轴上将向上移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,是某研究小组利用过氧化氢酶探究H2O2分解条件而获得的实验结果。相关叙述错误的是( )

A.图一可以得出酶具有高效性
B.图一bc段产生的原因可能是底物数量(浓度)有限
C.图二bc段产生的原因可能是过氧化氢酶数量(浓度)有限
D.图三可以得出pH越小或越大酶活性越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e五种元素在周期表前四周期的位置如下图所示,下列说法正确的是

A. 元素b位于VIA族,有+6、-2两种常见化合价
B. 元素c的气态氢化物的稳定性比元素b的强
C. 元素b、c、d的原子半径大小顺序:r(d)>r(c)>r(b)
D. 元素e的单质可能是一种半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com