
(14分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
(1)甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中。你认为甲同学在实验中应该观察到的现象是__________________________。
(2)乙同学为验证Fe在冷的浓HNO3中发生钝化但能和热的浓HNO3反应,设计了如图所示的实验,请你指出其中的两处错误:____________________________、_________________________;纠正上述错误后,请你从绿色化学的角度出发,对装置2提出改进建议,使装置2既能控制反应的进行,又能减少氮氧化物的排放:__________________________________________.
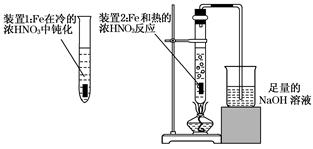
(3)丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后不再溶解(Cu有剩余)。
①丙同学依据反应现象得出Cu片溶解的原因是和HNO3发生反应.他依据的反应现象是___________。
②丁同学认为丙同学的结论不完全正确.他的理由是_________________________.
(4)请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象_________________________________________。
(每空2分,共14分)
(1)Cu能在Cl2中燃烧,产生棕黄色的烟
(2)两支试管中的液体均超过试管容积的三分之一
加热液体的试管应与桌面成45°角,向上倾斜而不应垂直向上
将装置2中的铁片改成一段为螺旋状的铁丝,螺旋状的一段深入硝酸中,另一端伸出橡皮塞
(3)①试管上部出现红棕色气体 ②Fe和硝酸反应后的溶液中可能有HNO3,但也一定有Fe3+,Fe3+也能和Cu反应而使Cu片溶解
(4)取该溶液少许,滴加适量的KSCN溶液,不出现红色,再滴加适量新制氯水,出现红色
【解析】
试题分析:(1)铜在氧气中不燃烧,在氯气中能燃烧产生棕黄色烟,故选氯气.
(2)加热液体时,试管内的液体不能超过试管的三分之一,超过三分之一时,加热过程中容易产生暴沸,造成安全事故;加热液体的试管应与桌面成45°角向上倾斜,不能竖直向上;改进后的铜丝容易抽拉,即容易控制反应的进行,从而减少氮氧化物的排放;
故答案为:两只试管中的液体均超过试管容积的1/3;加热液体的试管应与桌面成45°角向上倾斜;既能控制反应的进行又能减少氮氧化物的排放.
(3)①二氧化氮能和水反应生成硝酸和一氧化氮,当溶液中硝酸过量时,抑制二氧化氮的溶解,所以可看到气体呈红棕色;
故答案为:试管上部出现红棕色气体.
②硝酸过量时,铁和硝酸反应生成三价铁,三价铁和铜能反应生成二价铁离子和铜离子,从而使铜片溶解,发生反应为
2Fe3++Cu=Cu2++2Fe2+.
故答案为:2Fe3++Cu=Cu2++2Fe2+.
(4)二氧化氮能发生可逆反应生成四氧化二氮,2NO2?N2O4,从而使收集的气体小于0.1mol.
故答案为:2NO2?N2O4。
考点:铜金属及其重要化合物的主要性质 铁的化学性质
点评:本题考查了常见金属铜和铁的化学性质,难度不大,写三价铁离子和铜反应的离子方程式时要注意电荷守恒。


科目:高中化学 来源: 题型:阅读理解
(16分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
(1)甲同学完成了Fe、Cu分别与S、Cl2反应的实验,下列物质中不可能为甲同学实验得到的生成物是
A.FeCl3B.FeCl2 C.CuCl2D.FeS
(2)乙同学为验证Fe能和热的浓HNO3反应,设计了如上图所示的实验装置,请说出装置B的作用: 。开始加热前 (填“有”或“无”)明显现象。
(3)当乙同学实验结束时,铁完全溶解,试管液面上方为无色气体,试管上部为红棕色气体,此时丙同学用所得的溶液进行如下实验和探究:
①在所得的溶液中加入一小块Cu片,结果Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解。丙同学依据反应现象得出Cu片溶解的原因可能是和过量的HNO3发生反应。他依据的反应现象是 ;该反应的离子方程式为 。你认为Cu片溶解是否还有另一原因,若有请用化学方程式表示其理由: (若无此空不填)
②请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象 。
③丙同学实验结束后加水稀释后得到溶液500mL,假设实验全过程硝酸只被还原成NO和
NO2共0.02 mol并测得溶液中Fe2+和Cu2+浓度均为0.02 mol/L,则NO3-的物质的量浓度为
mol/L。生成NO气体的体积为 _________________L(标准状况)。
(4)本次探究实验用掉密度为1.5g·cm-3质量分数为95%的浓硝酸3mL,超出实际参加反应的量其原因有(写出两点):① ②
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省大田第一中学高一第一学期联合命题考试化学试卷 题型:实验题
(16分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题: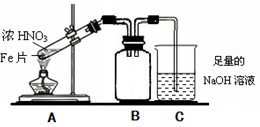
(1)甲同学完成了Fe、Cu分别与S、Cl2反应的实验,下列物质中不可能为甲同学实验得到的生成物是
| A.FeCl3 | B.FeCl2 | C.CuCl2 | D.FeS |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省忻州一中高一上学期期末联考化学试卷(A)(带解析) 题型:实验题
(14分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
(1)甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中。你认为甲同学在实验中应该观察到的现象是__________________________。
(2)乙同学为验证Fe在冷的浓HNO3中发生钝化但能和热的浓HNO3反应,设计了如图所示的实验,请你指出其中的两处错误:____________________________、_________________________;纠正上述错误后,请你从绿色化学的角度出发,对装置2提出改进建议,使装置2既能控制反应的进行,又能减少氮氧化物的排放:__________________________________________.
(3)丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后不再溶解(Cu有剩余)。
①丙同学依据反应现象得出Cu片溶解的原因是和HNO3发生反应.他依据的反应现象是___________。
②丁同学认为丙同学的结论不完全正确.他的理由是_________________________.
(4)请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象_________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省三明市普通高中高一上学期联合命题考试化学试卷 题型:实验题
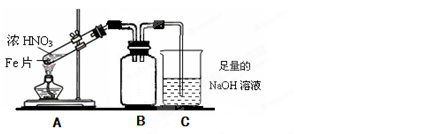
(16分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
(1)甲同学完成了Fe、Cu分别与S、Cl2反应的实验,下列物质中不可能为甲同学实验得到的生成物是
| A.FeCl3 | B.FeCl2 | C.CuCl2 | D.FeS |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com