
【题目】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是______________________。
在此过程中,两个电极上质量的变化值:阴极________阳极(填“>”“<”或“=”)。
(3)利用如图所示的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于________(填“M”或“N”)处。若X为锌,开关K置于M处,该电化学防护法称为________。

【答案】 2Al+3H2O-6e-===Al2O3+6H+ 能向电镀液中不断补充Cu2+,使电镀液中的Cu2+浓度保持恒定 = N 牺牲阳极的阴极保护法
【解析】试题分析:(1)铝材表面形成氧化膜,铝在阳极失电子发生氧化反应;(2) 铜作阳极,阳极反应为![]() =Cu2+;电镀铜时,阳极只发生
=Cu2+;电镀铜时,阳极只发生![]() =Cu2+反应;阴极只发生
=Cu2+反应;阴极只发生![]() =Cu;(3)若X为碳棒,开关K置于M处,构成原电池,铁是负极;若X为碳棒,开关K置于N处,构成电解池,铁是阴极。
=Cu;(3)若X为碳棒,开关K置于M处,构成原电池,铁是负极;若X为碳棒,开关K置于N处,构成电解池,铁是阴极。
解析:(1)铝材表面形成氧化膜,铝在阳极失电子发生氧化反应生成氧化铝,阳极电极反应式为2Al+3H2O-6e-===Al2O3+6H+;(2) 铜作阳极,能向电镀液中不断补充Cu2+,使电镀液中的Cu2+浓度保持恒定;电镀铜时,阳极只发生![]() =Cu2+反应;阴极只发生
=Cu2+反应;阴极只发生![]() =Cu;两个电极上质量的变化值:阴极=阳极。
=Cu;两个电极上质量的变化值:阴极=阳极。
(3)若X为碳棒,开关K置于M处,构成原电池,铁是负极,加快铁的腐蚀;若X为碳棒,开关K置于N处,构成电解池,铁是阴极,铁被保护。若X为碳棒,为减缓铁的腐蚀,开关K应置于N处。若X为锌,开关K置于M处,构成原电池,铁是正极,铁被保护,该电化学防护法称为牺牲阳极的阴极保护法。


科目:高中化学 来源: 题型:
【题目】在25℃时,向l0mL0.01mol·L-1NaA溶液中逐滴加入0.01mol·L-1的盐酸,滴定曲线如下图所示,下列说法正确的是( )

A. a点到c点的过程中,c(HA)+c(A-)=0.01mol·L-1等式始终成立
B. b点时,溶液中微粒浓度大小的关系:c(A-)>c(Cl-)>c(HA)>c(OH-)>c(H+)
C. c点溶液存在的关系:c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-)
D. 由图可知,等浓度的HA、NaA混合溶液中,HA的电离程度大于A-的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活密切相关,下列说法正确的是( )
A. 二氧化硫可广泛用于各类食品的漂白
B. 从海水提取任何物质都必须通过化学反应才能实现
C. 用热的纯碱溶液清除油圬
D. “地沟油”禁止食用,也不能用来制肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁电池是一种新兴的化学电源,总反应方程式:3Zn+2FeO42-+8H2O= 3Zn(OH)2↓+ 2Fe(OH)3↓+4OH-,其工作示意图如下。

下列说法不正确的是( )
A. Zn极上发生氧化反应
B. 电解质溶液中电子由左侧向右侧转移
C. 正极的电极反应式:FeO42-+3e-+4H2O=Fe(OH)3+5OH-
D. 反应一段时间后,Zn极质量减少6.5g,假设反应前后溶液体积不变仍为100 mL,则OH-浓度约增大了 1.33 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各对物质中,互为同系物的是
A. C2H4、C8H18 B. CH3CHO、C2H5OH C. C2H6、C4H10 D. CH3COOH、C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烃A为原料在隔绝空气、高温的条件下获得有机物B、C,有机物B、C、D、E、F之间的相互转化关系如下图。已知烃A在标准状况下的密度为l.96g·L-1,C 为天然气的主要成分,F有浓郁香味。
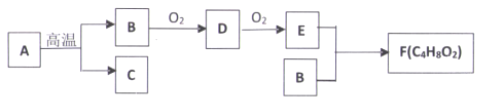
(1)有机物E中含有的官能团名称是_________。
(2)B+ E→F的反应类型是_________。
(3)有机物A在髙温下转化为B和C的化学方程式是_________。
(4)下列说法正确的是_________。
A.有机物A与C为同系物
B.有机物F可以在NaOH溶液中水解,属于皂化反应
C.有机物D可以和氢气发生加成反应
D.有机物A转化成B和C的反应在工业上用于提高汽油产量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请选择合适方法的填空(用字母序号填空):
A.过滤 B.裂解 C.分馏 D.裂化 E.干馏 F.还原 G.电解 H.蒸发
①从海水中提取粗盐__________________; ②重油转变为汽油_____________;
③石油炼制乙烯、丙烯等__________; ④煤转化为焦炭、煤焦油等____________。
(2)对于容积固定的反应:N2(g)+3H2(g) ![]() 2NH3(g)(正反应放热),达到平衡的标志有__________。
2NH3(g)(正反应放热),达到平衡的标志有__________。
A.N2、H2、NH3 的百分含量不再变化 B.总压强不变
C.N2、H2、NH3 的分子数之比为 1∶3∶2 D.N2、H2、NH3 的浓度相等
E.N2、H2 不再起反应 F.v(N2)=v(H2)
G.混合气体的密度不变 H.混合气体的平均相对分子质量不变
I.正反应放出的热量等于逆反应吸收的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com