
| A. | 碳酸钠是发酵粉的主要成分,而碳酸氢钠是治疗胃穿孔的一种药剂 | |
| B. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| C. | 大量生产一次性超薄塑料袋,方便人们日常生活 | |
| D. | 为补充人体所需的营养成分,人人都应食用添加营养强化剂的食品 |
分析 A.发酵粉的主要成分为碳酸氢钠;
B.硅酸钠溶液可用作阻燃剂;
C.可导致白色污染;
D.营养强化剂属于食品添加剂,不可随意使用.
解答 解:A.碳酸氢钠不稳定,易与酸反应,发酵粉的主要成分为碳酸氢钠,故A错误;
B.硅酸钠性质稳定,溶液可用作阻燃剂,故B正确;
C.塑料袋难以降解,可导致白色污染,应减少使用,故C错误;
D.食品营养强化剂是指“为增强营养成份而加入食品中的天然的或者人工合成的属于天然营养素范围的食品添加剂,食品添加剂不可滥用,要符合《食品营养强化剂使用卫生标准》,故D错误.
故选B.
点评 本题综合考查元素化合物知识,为高考成常见题型,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 钠离子与氯离子之间通过静电吸引结合在一起 | |
| B. | 与某个钠离子最接近的钠离子有12个 | |
| C. | 某个钠离子周围的氯离子围成的空间结构为正八面体 | |
| D. | 晶体中钠离子的半径比氯离子的半径小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S | B. | Al2S3 | C. | FeS | D. | CuS |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2 L N2含有的分子数为0.5 NA | |
| B. | 在常温常压下,1 mol 氦气含有的原子数为2NA | |
| C. | 在常温常压下,71 g Cl2所含原子数为2NA | |
| D. | 在同温同压时,相同体积的任何气体单质所含的原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
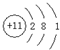 .C、D、E的简单离子半径由小到大的顺序Al3+<Na+<O2-( 用离子符号表示).
.C、D、E的简单离子半径由小到大的顺序Al3+<Na+<O2-( 用离子符号表示).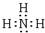 .检验该气体的常用方法是用润湿的红色石蕊试纸接近该气体,若试纸变蓝,证明氨气存在.
.检验该气体的常用方法是用润湿的红色石蕊试纸接近该气体,若试纸变蓝,证明氨气存在.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
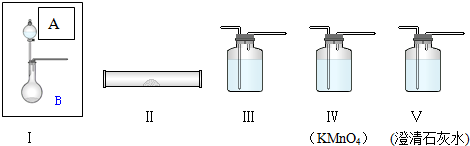
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com