
(1)C3H6O2有多种同分异构体,其中属于酯类且能发生银镜反应的有 个,写出其结构简式  。
。
(2)若用1 mol乙烯和足量的氯气在适当的条件下反应制取四氯乙烷,这一过程中所要经历的反应有 、 (填反应类型)及这一过程中耗用氯气 mol (反应产物中的有机物只有四氯乙烷)。
科目:高中化学 来源:2016届山西康杰中学等四校高三上第二次联考理化学试卷(解析版) 题型:填空题
阿司匹林口服时,具有解热镇痛作用。是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄。近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成。它的有效成分是乙酰水杨酸(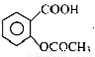 )。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐【(CH3CO)2O】为主要原料合成乙酰水杨酸。
)。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐【(CH3CO)2O】为主要原料合成乙酰水杨酸。
【反应原理及部分装置】
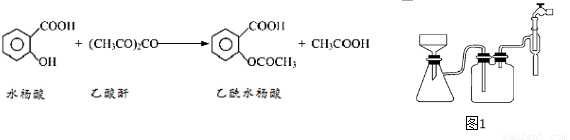
【实验流程】
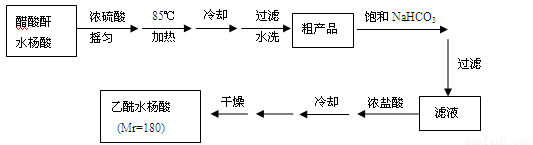
已知:①醋酸酐遇水分解生成醋酸。
②水杨酸和乙酰水杨酸均微溶于水,但其钠盐易溶于水,副产物为高分子化合物,难溶于水。
回答下列问题:
(1)合成过程中要控制温度在85℃~90℃,最合适的加热方法______。
(2)用图1装置过滤比普通漏斗过滤的优点是______________________。
(3)粗产品提纯:
①分批用少量饱和NaHCO3溶液溶解粗产品,目的是_______;判断该过程结束的现象是___________。
②加浓盐酸、冷却后的操作是__________、______、干燥、称重、计算产率。
③纯度检验:取少许产品加入盛有2 mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色。可能的原因是_____________。
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):
Ⅰ.称取阿司匹林样品mg;
Ⅱ.将样品研碎,溶于V1 mL a mol/LNaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;
Ⅲ.向锥形瓶中滴加几滴甲基橙,用浓度为b mol/L的标准盐酸滴定剩余的NaOH,消耗盐酸的体积为V2 mL。
已知 乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式:

则阿司匹林药片中乙酰水杨酸质量分数的表达式为:____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海西宁第十四中学高一上期中考试化学卷(解析版) 题型:选择题
下列化学反应,能用离子方程式H++OH- = H2O来表示的是( )
A. 盐酸和氢氧化铜 B. 硫酸和氢氧化钠溶液
C. 醋酸和氢氧化钡溶液 D. 稀硝酸和氨水混合
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海西宁第十四中学高二上期中考试化学卷(解析版) 题型:选择题
下列叙述正确的是
A.95 ℃纯水的pH<7,说明加热可导致水呈酸性
B.pH = 3的醋酸溶液,稀释至10倍后pH = 4
C.0.2 mol·L-1的盐酸,与等体积水混合后pH = 1
D.pH = 3的醋酸溶液,与pH = 11的氢氧化钠溶液等体积混合后pH = 7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏石嘴山第三中学高二上期中考试化学卷(解析版) 题型:选择题
苯酚和苯甲醇共同的化学性质是( )
A.具有酸性 B.与钠反应放出氢气
C.遇FeCl3溶液显紫色 D.与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源:2016届辽宁抚顺第一中学高三上第一次模拟考试化学试卷(解析版) 题型:选择题
下列有关物质分类会归类正确的一组是
①液氨、液氯、干冰、碘化银均为化合物
②漂白粉、盐酸、水玻璃、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④Na2O2、Na2CO3、Na2SiO3均为钠盐
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安第一中学高一上期中考试化学试卷(解析版) 题型:选择题
津冀地区遭遇三轮雾霾袭击,非常简洁地描述灰霾天气,就是“细粒子气溶胶粒子在高湿度条件下引发的低能见度事件”。气溶胶是胶体的一种,关于气溶胶,下列说法不正确的是( )
A.气溶胶的分散剂是气体
B.根据分散质和分散剂的状态,可以将胶体分为9种
C.气溶胶分散质粒子直径在1nm-100nm
D.胶粒不能透过滤纸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北衡水冀州中学高一上月考三理化学卷(解析版) 题型:推断题
I、A、B、C、D四种可溶性盐,其阳离子分别是Na+、Ba2+、Cu2+、Ag+ 中的某一种,阴离子分别是Cl-、SO42-、CO32-、NO3- 中的某一种。现做以下实验:
①将四种盐各取少量,分别溶于盛有5 mL蒸馏水的四支试管中,只有B盐溶液呈蓝色。
②分别向4支试管中加入2 mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述事实,推断这四种盐的化学式:A ,D ;
(2)写出实验步骤②中产生较多气泡现象的离子反应方程式: 。
II、用98%的浓硫酸(其密度为1.84 g/cm3) 配制100 mL 1.0 mol·L-1稀硫酸
实验步骤如下:① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④ 检漏、 转移、洗涤 ⑤ 定容、摇匀
若实验仪器有:
A 100 mL量筒 B 玻璃棒 C 50 mL容量瓶 D 100 mL容量瓶 E 10 mL量筒 F 胶头滴管 G 50 mL烧杯
回答下列问题:
(1)需量取浓硫酸的体积为__________mL。
(2)实验时不需选用的仪器有(填序号) _______________。
(3)配制过程中,下列情况会使配制结果偏高的是(填序号) _______________。
① 定容时俯视刻度线观察液面 ② 容量瓶使用时未干燥
③ 定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
④ 所用的浓硫酸长时间放置在密封不好的容器中
⑤ 用量筒量取浓硫酸时仰视读数
(4)检验试剂瓶中的溶液含有SO42- 的操作是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com