
| A. | 113号元素的相对原子质量为278 | |
| B. | 115号元素可显+5价 | |
| C. | ${\;}_{113}^{278}$Uut的中子数与电子数之差为165 | |
| D. | 两种元素均位于周期表第八周期 |
分析 A.元素的相对原子质量就是该元素各种同位素原子所占的一定百分比算出的平均值;
B.第七周期稀有气体原子序数=86+32=118,是第七周期最后一种元素,位于18列,115号元素处于第15列,故115号元素位于第七周期第ⅤA族,最外层电子数=主族序数;
C.原子符号左上角的数字表示质量数,左下角的数字表示质子数,中子数=质量数-质子数,核外电子数=质子数;
D.第七周期稀有气体原子序数=86+32=118,是第七周期最后一种元素,位于18列.
解答 解:A.核素${\;}_{113}^{278}$Uut的相对原子质量为278,不是113号元素的相对原子质量,故A错误;
B.115号元素位于第七周期第ⅤA族,最外层电子数=主族序数,所以115号元素可显+5价,故B正确;
C.${\;}_{113}^{278}$Uut的质子数为113,质量数为278,中子数=278-113=165,电子数为113,中子数与电子数差为165-113=52,故C错误;
D.第七周期稀有气体原子序数=86+32=118,是第七周期最后一种元素,位于18列,115号元素处于第15列,113号元素处于第13列,均位于周期表第七周期,故D错误;
故选B.
点评 本题考查元素周期表的结构与应用,题目难度中等,明确同位素及原子的构成、电子排布与元素的位置为解答的关键,注重基础知识的考查.


科目:高中化学 来源: 题型:选择题
| A. | 铜和稀硝酸反应 Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| B. | 碳酸氢钠的水解 HCO3-+H2O=H2CO3+OH- | |
| C. | Fe投入盐酸中 2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氢氧化铝溶于氢氧化钠溶液 Al(OH)3+OH-=AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
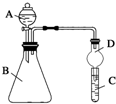 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 | |
| B. | 与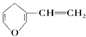 互为同分异构体的芳香族化合物有5种 互为同分异构体的芳香族化合物有5种 | |
| C. | 含有5个碳原子的饱和链烃,其一氯取代物有3种 | |
| D. | 菲的结构简式为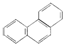 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
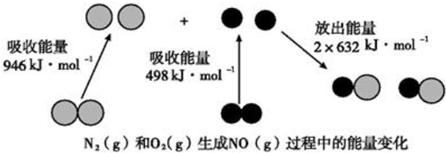
| A. | 1mol N2(g)和1mol O2(g)反应放出的能量为180kJ | |
| B. | 1mol N2(g)和1mol O2(g)具有的总能量小于2molNO(g)具有的总能量 | |
| C. | 该反应中反应物断开化学键所吸收的总能量小于生成物形成化学键所释放出的总能量 | |
| D. | 恒容密闭容器中,充入Ar气,该反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ($\frac{b}{10}$-$\frac{a}{20}$) mol•L-1 | B. | (2b-a) mol•L-1 | C. | (5b-$\frac{5a}{2}$) mol•L-1 | D. | (10b-5a) mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3的水溶液能导电,因此NH3是电解质 | |
| B. | 焰色反应是物理变化 | |
| C. | 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 | |
| D. | 蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com