
【题目】下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。回答问题:
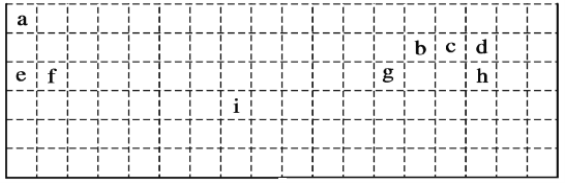
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。并注明金属非金属的分界线___。
(2)有人认为在元素周期表中,有一种元素也可以放在第ⅦA族,你认为该元素为___(填元素符号)。
(3)实验室制ca3的化学反应方程式为___。
(4)g的氧化物与e的最高价氧化物对应水化物反应的离子方程式为___。
(5)设计实验验证b、c非金属性的强弱,用离子方程式表示为___。
(6)i在周期表中的位置为___。i对应的单质与水反应的化学方程式为___。
(7)a2d2的电子式为___;用电子式表示fCl2的形成过程___。
(8)分别由a、d、e、h四种元素形成的两种盐反应的离子方程式为___。
【答案】 H Ca(OH)2+2NH4Cl
H Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑ Al2O3+2OH-=2AlO2-+H2O CO32-+2H+=CO2↑+H2O 第四周期第Ⅷ族 3Fe+4H2O(g)
CaCl2+2H2O+2NH3↑ Al2O3+2OH-=2AlO2-+H2O CO32-+2H+=CO2↑+H2O 第四周期第Ⅷ族 3Fe+4H2O(g)![]() Fe3O4+4H2↑
Fe3O4+4H2↑ ![]()
![]() H++HSO3-=H2O+SO2↑
H++HSO3-=H2O+SO2↑
【解析】
(1)用实线是元素周期表的部分边界,用红线表示金属与非金属的分界线为: ;
;
(2)第ⅦA族元素容易得一个电子,显-1价,而H也可以显-1价,如在NaH中H的化合价为-1,应该是H;
(3)c为N,a为H,则ca3是NH3,实验室制法:Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;
(4)g是Al,则其氧化物为Al2O3,e是Na,其最高价氧化物对应水化物为NaOH,反应的离子方程式为:Al2O3+2OH-=2AlO2-+H2O;
(5)b是C、c是N,比较非金属性的强弱,可比较最高价氧化物对应水化物酸性,酸性:HNO3>H2CO3,离子方程式为:CO32-+2H+=CO2↑+H2O;
(6)i为铁,为于第四周期第Ⅷ族,与水的反应为:3Fe+4H2O(g)![]() Fe3O4+4H2↑;
Fe3O4+4H2↑;
(7)b是O,则a2d2是H2O2,双氧水为共价化合物,分子中存在两个H-O键和一个O-O键,电子式为![]() ;f是Mg,fCl2是MgCl2,用电子式表示MgCl2的形成过程为:
;f是Mg,fCl2是MgCl2,用电子式表示MgCl2的形成过程为:![]() ;
;
(8)分别由a、d、e、h四种元素形成的两种盐分别是NaHSO3、NaHSO4,反应的离子方程式为:H++HSO3-=H2O+SO2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定量的CH4燃烧后得到的产物是CO、CO2、H2O(g),此混合物的质量为49.6 g,当其缓缓通过足量的无水CaCl2时气体质量减少25.2 g,则混合气中CO的质量为( )。
A. 24.4 gB. 13.2 gC. 12.5 gD. 11.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学生用如图装置研究原电池原理,下列说法错误的是( )
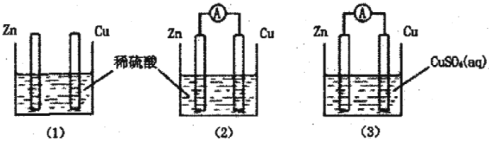
A.(2)图中电子由Zn沿导线流向Cu
B.(3)图中Zn片增重质量与Cu棒减轻质量比值为65∶64
C.(1)图中铜棒上没有气体产生
D.(2)图与(3)图中正极生成物质量比为1∶32时,Zn片减轻的质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。
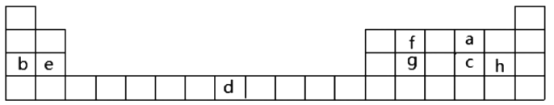
(1)表中字母h元素在周期表中位置___。
(2)写出b元素的最高价氧化物对应的水化物所含化学键类型___。
(3)下列事实能说明a元素的非金属性比c元素的非金属性强的有___。
A.a单质与c的氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mola单质比1molc单质得电子数目多
C.a和c两元素的简单氢化物受热分解,前者的分解温度高
(4)g与h两元素的单质反应生成1molg的最高价化合物。恢复至室温,放热687kJ。已知该化合物的熔、沸点分别为-69℃和58℃。写出该反应的热化学方程式___。
(5)常温下d遇浓硫酸形成致密氧化膜,若薄膜为具有磁性的该元素氧化物,写出该反应的化学方程式___。
(6)e与f形成的1mol化合物Q与水反应,生成2mol氢氧化物和1mol烃,该烃分子中碳氢质量比为9∶1,写出烃分子电子式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、M均为短周期元素,M的一种核素不含中子,X、Y、Z、W在周期表中的位置如图所示,Y原子最外层电子数为内层电子数的3倍。下列说法不正确的是
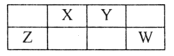
A. 原子半径:Z>X>Y>M
B. X、Y、Z、W与M均能形成18电子分子
C. X、Y、M形成的化合物水溶液一定呈酸性
D. Y的简单阴离子还原性弱于X的简单阴离子还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖不仅是重要的营养物质,而且还能转化成其他重要的调味品。以淀粉为原料在一定条件下可获得有机物葡萄糖、A、B、C、D,其相互转化关系如图。已知C不能发生银镜反应,D为有浓郁香味,不溶于水的油状液体。
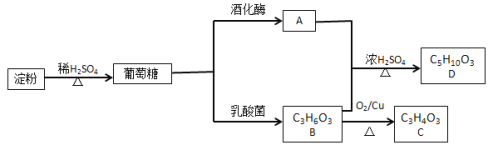
请回答:
(1)与A互为同分异构体的结构式________。
(2) B→C的反应类型是________。
(3) A+ B→D的化学方程式是________________________。
(4) 下列说法正确的是________。
A 有机物A与金属钠反应比水与金属钠反应要剧烈
B 有机物A、B、D可用饱和Na2CO3溶液鉴别
C 两分子B在浓硫酸作用下可以形成六元环状化合物
D 往淀粉水解液中,加入足量的NaOH溶液,再加入碘水,如果溶液未变蓝色,则说明淀粉水解完成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示下列描述正确的是

A. 反应开始到10s,用Z表示的反应速率为0.158 mol/(Ls)
B. 反应开始到10s,X的物质的量浓度减少了0.79 mol/L
C. 反应开始到10s,Y的转化率为79.0 %
D. 反应的化学方程式为:X+Y![]() Z
Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一氧化碳变换反应CO + H2O![]() CO2 + H2中,有关反应条件改变使反应速率增大的原因分析不正确的是
CO2 + H2中,有关反应条件改变使反应速率增大的原因分析不正确的是
A.使用催化剂,活化分子百分数增大,有效碰撞几率增加
B.升高温度,活化分子百分数增大,有效碰撞几率增加
C.增大压强,单位体积内活化分子数增多,有效碰撞几率增加
D.增大c(CO),活化分子百分数增大,有效碰撞几率增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
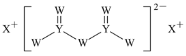
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W分别与X、Y、Z形成的二元化合物均只有一种
D.化合物M中W不都满足8电子稳定结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com