

| A.原子半径:Y>Z>W |
| B.XW2熔点为—107℃,沸点为12.5℃,说明固态XW2为分子晶体 |
| C.YW3水溶液蒸干并灼烧可得YW3固体 |
| D.ZW2分子结构如右图,说明ZW2是极性分子 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(A-x+n) mol | B.(A-x-n) mol |
C.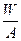 (A-x+n) mol (A-x+n) mol | D.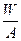 (A-x-n) mol (A-x-n) mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
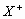 和
和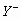 两种离子具有相同的电子层结构;
两种离子具有相同的电子层结构;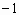 价阴离子。
价阴离子。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同周期元素的原子半径以ⅦA族的为最大 |
| B.同主族两种元素原子的核外电子数的差值可能为26 |
| C.短周期中次外层电子数是最外层电子数2倍的原子一定是非金属元素 |
| D.科学家在周期表中金属与非金属分界线处找到了优良的催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1S22S22P63S23P64S 1与1S22S22P63S1 |
| B.1S22S22P63S2与1S22S22P63S23P1 |
| C.1S22S22P63S23P4与1S22S22P6 |
| D.1S22S22P2与1S22S22P5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.XY晶体一定是离子晶体 |
| B.若Y的原子序数为m,X的原子序数一定是m±6 |
| C.X、Y可以属于同一周期,也可属于两个不同周期 |
| D.X与Y一定不属于同一主族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com